题目内容
1.实验室部分仪器或装置如图所示,请回答下列问题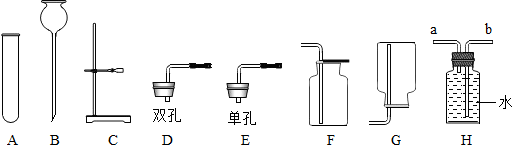
(1)实验室常用石灰石和稀盐酸制取二氧化碳气体,反应方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;.
若要组装一套二氧化碳的发生装置,可选择图中的ACE(填仪器下方的字母,下同),收集装置可选用图中的F.
(2)用该发生装置还可以制取的气体是氧气,(填一种)反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(3)若用装置H收集氧气,氧气应从a(填“a”或“b”)端导入.
分析 (1)根据实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,大理石和石灰石的主要成分是碳酸钙,通常情况下,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;二氧化碳能够溶于水,密度比空气大解答;
(2)根据用过氧化氢和二氧化锰制氧气,不需要加热的仪器,常温进行解答;
(3)根据氧气的性质解答.
解答 解:
(1)实验室制取CO2的反应物是碳酸钙与稀盐酸,生成物是氯化钙、水、二氧化碳,方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;实验室制取二氧化碳属于固液常温型,所以选择试管、铁架台、单孔塞,二氧化碳的密度比空气大且能溶于水,所以可用向上排空气法收集;
(2)用过氧化氢和二氧化锰制氧气,不需要加热的仪器;,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,配平即可;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)用H装置收集氧气,氧气的密度小于水的密度,所以氧气应从a端导入.
答案:
(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;ACE F
(2)氧气 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)a
点评 固液常温型装置可用试管、单孔橡皮塞装置或长颈漏斗装置,固体加热型装置需用到酒精灯,气体的收集方法根据其密度和水溶性判断.

练习册系列答案
相关题目
9.下表是元素周期表中第三周期元素的原子结构示意图.

依据上表判断,下列结论正确的是( )

依据上表判断,下列结论正确的是( )
| A. | 11号元素的原子,在化学反应中容易得到电子变成离子 | |
| B. | 铝元素与氧元素形成化合物的化学式为 Al3O2 | |
| C. | 上述元素称为第三周期元素是因为这些元素的原子核外都有三个电子层 | |
| D. | Cl→Cl-,则 Cl 核内有 18 个质子 |
16.下列各组离子在溶液中一定能大量共存的是( )
| A. | H+、CO32-、K+、Cl- | B. | H+、Na+、Cl-、NO3- | ||
| C. | Ba2+、Cu2+、SO42-、Cl- | D. | Mg2+、Ba2+、OH-、CO32- |
13. 纳来球异质二聚体是纳米自动化产业中的一种新模型.不溶于水的二氧化硅晶体可以制成微小的纳米球.在铂的催化作用下,双氧水分解,同时使一个二氧化硅纳米球与一个铂纳米球相结合,构成了一个纳米球异质二聚体(如右下图所示),这就是一个纳米级发动机.它可望用于河流和溪水的污染控制以及人体内部器官和细胞的运行.根据以上信息判断,下列说法正确的是( )
纳来球异质二聚体是纳米自动化产业中的一种新模型.不溶于水的二氧化硅晶体可以制成微小的纳米球.在铂的催化作用下,双氧水分解,同时使一个二氧化硅纳米球与一个铂纳米球相结合,构成了一个纳米球异质二聚体(如右下图所示),这就是一个纳米级发动机.它可望用于河流和溪水的污染控制以及人体内部器官和细胞的运行.根据以上信息判断,下列说法正确的是( )
 纳来球异质二聚体是纳米自动化产业中的一种新模型.不溶于水的二氧化硅晶体可以制成微小的纳米球.在铂的催化作用下,双氧水分解,同时使一个二氧化硅纳米球与一个铂纳米球相结合,构成了一个纳米球异质二聚体(如右下图所示),这就是一个纳米级发动机.它可望用于河流和溪水的污染控制以及人体内部器官和细胞的运行.根据以上信息判断,下列说法正确的是( )
纳来球异质二聚体是纳米自动化产业中的一种新模型.不溶于水的二氧化硅晶体可以制成微小的纳米球.在铂的催化作用下,双氧水分解,同时使一个二氧化硅纳米球与一个铂纳米球相结合,构成了一个纳米球异质二聚体(如右下图所示),这就是一个纳米级发动机.它可望用于河流和溪水的污染控制以及人体内部器官和细胞的运行.根据以上信息判断,下列说法正确的是( )| A. | 二氧化硅纳米球中含有的硅、氧原子个数比不为1:2 | |
| B. | 纳米球异质二聚体,其微粒大小在纳米级范围 | |
| C. | 双氧水分解时,二氧化硅是催化剂 | |
| D. | 因为二氧化硅晶体能与水反应而溶解,所以该纳米级发动机可以用于水污染的控制 |
10.下列试剂瓶的标签,化学式书写正确的是( )
| A. | 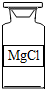 | B. | 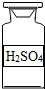 | C. | 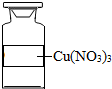 | D. |  |
11.二氧化碳和氢气可在一定条件下反应生成一种重要的化工原料甲醇,反应的化学方程式为:CO2+3H2$\frac{\underline{\;钌-膦铬合物\;}}{加压}$CH3OH+H2O.下列有关该反应的说法正确的是( )
| A. | 钌-膦铬合物的质量在反应前后发生了变化 | |
| B. | 氢原子数在反应前后发生了改变 | |
| C. | 为CO2的利用创造了一种新途径 | |
| D. | 属于复分解反应 |
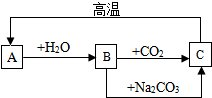 A、B、C是三种常见的含钙化合物,它们之间有如图所示的转化关系(部分产物略去):
A、B、C是三种常见的含钙化合物,它们之间有如图所示的转化关系(部分产物略去):