题目内容
13.如图的反应中,甲、乙、丙三种分子的个数比为1:3:2,则从图示中获得的信息正确的是( )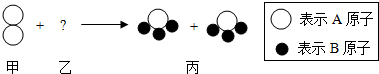
| A. | 生成物一定属于氧化物 | B. | 原子种类在化学反应中发生了变化 | ||
| C. | 该反应不可能是分解反应 | D. | 乙分子中A与B的原子个数比为1:2 |
分析 根据化学变化前后原子的种类和数目不变,由甲、乙、丙三种分子的个数比为1:3:2,结合反应的微观示意图可推断:每个乙分子由两个●--B原子构成;利用完善后的微观反应示意图,完成对所得信息的判断.
解答 解:化学变化前后原子的种类和数目不变,由甲、乙、丙三种分子的个数比为1:3:2,结合反应的微观示意图可推断:每个乙分子由两个●--B原子构成,据示意图可以看出,该反应是A2+3B2=2AB3,
A、该生成物是由两种元素组成,但不一定含有氧元素,因此不一定是氧化物,故选项错误;
B、反应前后分子改变,而原子的种类不变,故选项错误;
C、根据分子结构图及方程式可知该反应为两种物质生成一种物质的化合反应,因此不可能是分解反应;故选项错误;
D、根据微观示意图及化学反应前后原子的种类和个数都不变可知每个乙分子由两个●--B原子构成,没有A原子,故选项错误;
故选项为:C.
点评 本题考查的是化学反应的微观模拟表示,解答本题的关键是根据图示写出反应的化学方程式,然后做出正确的判断,并熟知化学反应的实质是分子破裂为原子,原子重新组成新的分子,化学变化前后原子的种类、数目不变,分子的种类一定改变.

练习册系列答案
相关题目
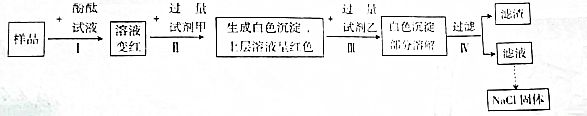
4.设计一个优化的实验方案,验证某氯化钠溶液中混有碳酸钠、硫酸钠和氢氧化钠并提纯氯化钠,其实验流程及部分实验现象如图所示.下列说法不正确的是( )
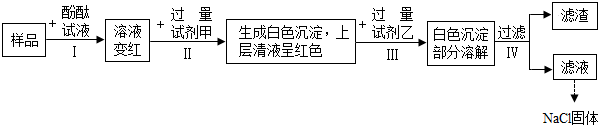

| A. | 样品溶液的pH大于7 | |
| B. | 试剂甲是BaCl2溶液 | |
| C. | 第Ⅲ步实验中还观察到的现象是有气泡产生 | |
| D. | 最后一步所得滤液含有的溶质是NaCl,BaCl2,HCl(指示剂除外) |
8.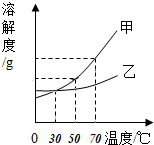 甲、乙两种物质的溶解度曲线如图所示,70℃时,将等质量的甲、乙两种固体(不含结晶水)分别加入到各盛100g水的两个烧杯中,充分搅拌固体均完全溶解,降温到50℃,观察到甲的溶液中固体析出.下列说法不正确的是( )
甲、乙两种物质的溶解度曲线如图所示,70℃时,将等质量的甲、乙两种固体(不含结晶水)分别加入到各盛100g水的两个烧杯中,充分搅拌固体均完全溶解,降温到50℃,观察到甲的溶液中固体析出.下列说法不正确的是( )
 甲、乙两种物质的溶解度曲线如图所示,70℃时,将等质量的甲、乙两种固体(不含结晶水)分别加入到各盛100g水的两个烧杯中,充分搅拌固体均完全溶解,降温到50℃,观察到甲的溶液中固体析出.下列说法不正确的是( )
甲、乙两种物质的溶解度曲线如图所示,70℃时,将等质量的甲、乙两种固体(不含结晶水)分别加入到各盛100g水的两个烧杯中,充分搅拌固体均完全溶解,降温到50℃,观察到甲的溶液中固体析出.下列说法不正确的是( )| A. | 降温到50℃时乙的溶液一定有固体析出 | |
| B. | 70℃时所得甲和乙的溶液一定都是不饱和溶液 | |
| C. | 若从50℃再降温到30℃,甲和乙的溶液均继续析出固体 | |
| D. | 降温到30℃后,两溶液中溶质的质量分数相等 |
18.化学用语是学习化学的重要工具,按要求用化学用语填空:
(1)2个氮分子2N2;
(2)2个硫酸根离子2SO42-;
(3)医疗上用来治疗胃酸过多的一种盐NaHCO3;
(4)常见钾肥KCl(任写一种).
(1)2个氮分子2N2;
(2)2个硫酸根离子2SO42-;
(3)医疗上用来治疗胃酸过多的一种盐NaHCO3;
(4)常见钾肥KCl(任写一种).
5.下列食物中富含蛋白质的是( )
| A. | 米饭馒头 | B. | 红烧鲤鱼 | C. | 凉拌黄瓜 | D. | 红薯粉条 |
3.NaOH、Na2CO3、NaCl在不同溶剂中的溶解度如下表所示.
表1 NaOH、Na2CO3、NaCl分别在水中的溶解度(S/g)
表2 常温下,NaOH、Na2CO3、NaCl分别在乙醇中的溶解度(S/g)
根据表1和表2提供的数据回答下列问题:
(1)NaOH在水中的溶解度随温度升高而增大(填“增大”或“减小”)
(2)20℃时,饱和食盐水中溶质的质量分数为26.5%(计算结果精确到0.1%);
(3)为证明CO2能与NaOH发生反应,小明同学将CO2通入饱和NaOH的乙醇溶液中.请推测该实验可观察到的现象溶液变浑浊,推测依据是碳酸钠在乙醇中的溶解度很小.
表1 NaOH、Na2CO3、NaCl分别在水中的溶解度(S/g)
| t/℃ | NaOH | Na2CO3 | NaCl |
| 0 | 42 | 7.1 | 35.7 |
| 10 | 51 | 12.2 | 35.8 |
| 20 | 109 | 21.8 | 36.0 |
| 30 | 119 | 39.7 | 36.3 |
| NaOH | Na2CO3 | NaCl |
| 17.3 | <0.01 | 0.1 |
(1)NaOH在水中的溶解度随温度升高而增大(填“增大”或“减小”)
(2)20℃时,饱和食盐水中溶质的质量分数为26.5%(计算结果精确到0.1%);
(3)为证明CO2能与NaOH发生反应,小明同学将CO2通入饱和NaOH的乙醇溶液中.请推测该实验可观察到的现象溶液变浑浊,推测依据是碳酸钠在乙醇中的溶解度很小.
 某实验小组利用如图所示装置测量空气中氧气体积分数并取得成功.
某实验小组利用如图所示装置测量空气中氧气体积分数并取得成功.