题目内容
18. 如图是小柯同学在复习科学时,构建酸通性的“手掌图”,其中五个手指表示能与酸发生化学反应的五类物质.
如图是小柯同学在复习科学时,构建酸通性的“手掌图”,其中五个手指表示能与酸发生化学反应的五类物质.(1)无名指上漏填的一类物质是碱.
(2)若利用铜来制取硫酸铜,常用的方法是:铜$\stackrel{步骤①}{→}$氧化铜$\stackrel{步骤②}{→}$硫酸铜,请你写出步骤②反应的化学方程式H2SO4+CuO═CuSO4+H2O.
分析 (1)根据酸的通性分析解答;
(2)根据化学方程式的书写步骤书写
解答 解:(1)根据酸的性质可以知道:酸溶液能跟酸碱指示剂、多种活泼金属、金属氧化物、碱以及某些盐反应,故无名指上漏填的一类物质是碱;
(2)氧化铜可以和稀硫酸反应生成蓝色的硫酸铜溶液,该反应的化学方程式为:H2SO4+CuO═CuSO4+H2O;
故答案为:(1)碱;
(2)H2SO4+CuO═CuSO4+H2O.
点评 掌握酸的通性和化学方程式的书写是解题的关键.

练习册系列答案
相关题目
13.据报道,我国长征五号“冰箭”运载火箭将于今年9月试射,这种无污染的火箭采用液氢和液氧作为推进剂,其中液氧属于( )
| A. | 单质 | B. | 氧化物 | C. | 化合物 | D. | 混合物 |
3.环境保护是2016年两会热点话题,下列说法错误的是( )
| A. | 使用无磷洗衣粉预防水体富营养化 | |
| B. | 淘汰黄标车减少汽车尾气污染 | |
| C. | 深埋废旧电池减少重金属污染 | |
| D. | 使用低毒、低残留农药减轻环境污染 |
7.茶叶中的单宁酸具有抑制血压上升、清热解毒、抗癌等功效,其化学式为C76H52O46,下列说法错误的是( )
| A. | 单宁酸由C、H、O三种元素组成 | |
| B. | 单宁酸中氢元素质量分数最小 | |
| C. | 单宁酸中氢、氧元素的质量比为26:23 | |
| D. | 单宁酸是有机化合物 |
12.盛碱液的试剂瓶若使用磨砂玻璃塞,时间长了可能生成Na2SiO3,而使瓶塞被粘住,则Na2SiO3中Si元素的化合价为( )
| A. | -2 | B. | +2 | C. | +6 | D. | +4 |
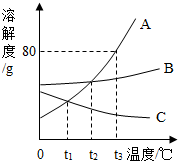 如图是A、B、C三种固体物质的溶解度曲线图,请结合图示回答下列问题:
如图是A、B、C三种固体物质的溶解度曲线图,请结合图示回答下列问题: