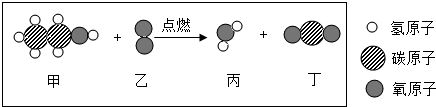
题目内容
16.在A+B→盐+水的反应中,A、B分别是( )| A. | 熟石灰和氯化铵 | B. | 纯碱和熟石灰 | C. | 小苏打和盐酸 | D. | 硫酸和熟石灰 |
分析 知道反应的产物的情况,结合物质的分类,判断是否是盐与水两种物质生成,从而进行分析判断.
解答 解:A、熟石灰与氯化铵反应会生成氨气水与氯化钙三种物质,故A错误;
B、纯碱与熟石灰反应时会生成碳酸钙与氢氧化钠,是盐与碱,故B错误;
C、小苏打与盐酸反应会生成水、二氧化碳和氯化钠三种物质,故C错误;
D、硫酸与熟石灰反应时会生成硫酸钙与水,属于盐和水,故D正确.
故选:D.
点评 本题是一道酸碱盐之间反应的题目,解题时只要抓住要求反应的特点,对各反应的生成物进行分析即可.

练习册系列答案
相关题目
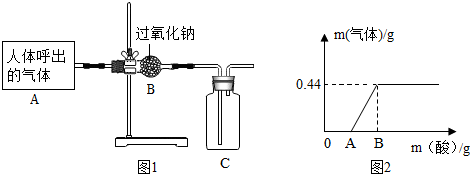
6.过氧化钠(Na2O2)是一种淡黄色粉末,可作为潜水艇或呼吸面具有供氧剂.人呼出气体的主要成份有氮气、氧气、二氧化碳和水蒸气,二氧化碳和水能分别与Na2O2反应生成氧气.为了探究Na2O2在潜水艇中反应后的物质,明明同学设计了如图1所示模拟实验.
【猜想与假设】
(1)明明猜想生成的固体物质是:(Ⅰ)氢氧化钠(Ⅱ)碳酸钠(Ⅲ)氢氧化钠和碳酸钠
【实验与验证】
(2)明明通过以下实验探究来验证他的猜想:
实验①:取少量反应后干燥管中的固体样品,置于试管中,向其中加入稀盐酸,发现有气泡产生,该气体通入澄清石灰水,石灰水变浑浊,证明猜想(Ⅰ)不成立.
实验②:取少量反应后干燥管中的固体样品,置于试管中,加水溶解,配成溶液,再用洁净干燥的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=10,证明猜想(Ⅱ)不成立.对他的操作方法、测量结果及结论的评价,正确的是C.
A.方法正确,结果正确,且结论正确 B.方法不正确,结果偏大,但结论正确
C.方法不正确,结果偏小,结论不正确 D.方法正确,结果正确,但结论不正确
实验③:继续探究,请将明明的探究过程填写完整.
于是明明得出结论:猜想(Ⅱ)不成立,猜想(Ⅲ)成立.该样品中含氢氧化钠的原因(用化学方程式表示)2NaOH+CO2=Na2CO3+H2O.
【反思与评价】
(3)明明认为碳酸钠一定是Na2O2与呼出气体中的二氧化碳反应生成的,因为过氧化钠和二氧化碳反应生成碳酸钠和氧气;他认为也可在上述实验装置中的A、B之间增加一个装有浓硫酸的干燥装置,重复实验①即可证明自己的判断.
【拓展与延伸】
(4)明明另取少量反应后干燥管中的固体样品,配制成溶液,向其中逐滴滴加稀盐酸,产生气体的质量与加入稀盐酸的质量的关系如图2所示.
①开始滴加盐酸时没有产生气体的原因是盐酸与氢氧化钠发生了反应.
②计算该样品中碳酸钠的质量;
③若A为10克,B为20克,则所用稀盐酸的溶质的质量分数为多少?

【猜想与假设】
(1)明明猜想生成的固体物质是:(Ⅰ)氢氧化钠(Ⅱ)碳酸钠(Ⅲ)氢氧化钠和碳酸钠
【实验与验证】
(2)明明通过以下实验探究来验证他的猜想:
实验①:取少量反应后干燥管中的固体样品,置于试管中,向其中加入稀盐酸,发现有气泡产生,该气体通入澄清石灰水,石灰水变浑浊,证明猜想(Ⅰ)不成立.
实验②:取少量反应后干燥管中的固体样品,置于试管中,加水溶解,配成溶液,再用洁净干燥的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=10,证明猜想(Ⅱ)不成立.对他的操作方法、测量结果及结论的评价,正确的是C.
A.方法正确,结果正确,且结论正确 B.方法不正确,结果偏大,但结论正确
C.方法不正确,结果偏小,结论不正确 D.方法正确,结果正确,但结论不正确
实验③:继续探究,请将明明的探究过程填写完整.
| 实验操作 | 现象或测定结果 | 结论 |
| 步骤1:取少量反应后干燥管中的固体样品溶于水配成溶液,滴加过量的氯化钙溶液,充分反应后过滤 | 有白色沉淀生成 | 该样品中有碳酸钠 |
| 步骤2:用PH试纸测定步骤1所得滤液的酸碱度. | pH>7 | 该样品中含有氢氧化钠 |
【反思与评价】
(3)明明认为碳酸钠一定是Na2O2与呼出气体中的二氧化碳反应生成的,因为过氧化钠和二氧化碳反应生成碳酸钠和氧气;他认为也可在上述实验装置中的A、B之间增加一个装有浓硫酸的干燥装置,重复实验①即可证明自己的判断.
【拓展与延伸】
(4)明明另取少量反应后干燥管中的固体样品,配制成溶液,向其中逐滴滴加稀盐酸,产生气体的质量与加入稀盐酸的质量的关系如图2所示.
①开始滴加盐酸时没有产生气体的原因是盐酸与氢氧化钠发生了反应.
②计算该样品中碳酸钠的质量;
③若A为10克,B为20克,则所用稀盐酸的溶质的质量分数为多少?
7.下列除去杂质(括号内为杂质)的方法正确的是( )
| A. | CO(CO2):通过灼热的氧化铜 | B. | MgSO4 (CuSO4):加入适量的氢氧化镁 | ||
| C. | KNO3溶液(NaCl):降温结晶 | D. | 铁粉(氧化铜粉末):加入足量稀硫酸 |
4.科学实验中,药品和仪器的存放应符合一定的规范.下列物质存放在对应的容器中,不符合规范的是( )
| A. |  浓硫酸 | B. |  石灰石 | C. |  稀盐酸 | D. |  氢氧化钠溶液 |
11.化学实验活动课上,同学们利用如图实验探究氢氧化钙的性质.
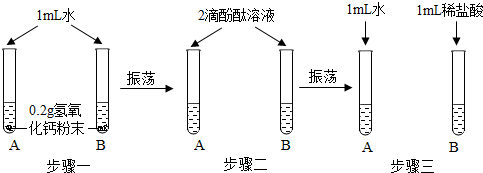
(1)写出步骤三试管B中发生的化学反应方程式:Ca(OH)2+2HCl═CaCl2+2H2O;
(2)上述三个步骤的A试管中的固体始终无明显减少,那么能说明A试管中溶有氢氧化钙的现象是步骤二中的A试管变红色;
(3)以上实验结束后,B试管中的固体消失,溶液澄清并无色.
【提出问题】步骤三B试管的溶液中,除指示剂外,溶质的成分还有什么?
【猜想】猜想一:溶质为CaCl2、HCl;
猜想二:溶质CaCl2、Ca(OH)、HCl;
猜想三:溶质为:只有CaCl2.
【小组讨论】同学们经过讨论得出猜想二一定是错误的.
【实验探究】小红同学利用了下面的实验验证了猜想一.
用试纸测溶液的PH操作是用干净的玻璃棒蘸取待测溶液并滴在pH试纸上,把试纸显示的颜色与标准比色卡对照,读出相同颜色的pH值.
(4)固体氢氧化钙露置空气中一段时间会变质的,原因是:Ca(OH)2+CO2═CaCO3+H2O(用方程表示).

(1)写出步骤三试管B中发生的化学反应方程式:Ca(OH)2+2HCl═CaCl2+2H2O;
(2)上述三个步骤的A试管中的固体始终无明显减少,那么能说明A试管中溶有氢氧化钙的现象是步骤二中的A试管变红色;
(3)以上实验结束后,B试管中的固体消失,溶液澄清并无色.
【提出问题】步骤三B试管的溶液中,除指示剂外,溶质的成分还有什么?
【猜想】猜想一:溶质为CaCl2、HCl;
猜想二:溶质CaCl2、Ca(OH)、HCl;
猜想三:溶质为:只有CaCl2.
【小组讨论】同学们经过讨论得出猜想二一定是错误的.
【实验探究】小红同学利用了下面的实验验证了猜想一.
| 实验操作 | 实验现象 | 实验结论 |
| 用广泛pH试纸检测步骤三B试管中溶液的pH | pH=5,则溶液呈酸性 | 猜想一正确 |
(4)固体氢氧化钙露置空气中一段时间会变质的,原因是:Ca(OH)2+CO2═CaCO3+H2O(用方程表示).
8.归纳与反思是学习化学的重要环节.下列各项归纳完全正确的是( )
| A.物质的鉴别 | B.能源与环境 |
| 软水和硬水--肥皂水 天然纤维和合成纤维--灼烧 | 使用氢能源--无污染 使用乙醇汽油--无污染 |
| C.性质与用途 | D.营养与健康 |
| 氧气有助燃性--做燃料 熟石灰呈碱性--改良酸性土壤 | 人体缺维生素C--易患坏血病 牛奶保鲜--加微量防腐剂 |
| A. | A | B. | B | C. | C | D. | D |
5.控制变量法是实验探究的重要方法,下列实验方法的设计中,能达到实验目的是( )


| A. | 图甲比较铁、铜的金属活动性强弱 | |
| B. | 图乙探究金属的锈蚀是否需要水 | |
| C. | 图丙探究MnO2对H2O2分解的催化作用 | |
| D. | 图丁探究可燃物的燃烧是否需要达到一定温度 |