题目内容
4.遂川“狗牯脑”茶叶享誉天下,茶叶中含有丰富的有机物和无机物,某化学研究小组测定茶叶中钙元素含量的实验方案如下:【查阅资料】
(1)茶叶中铝、铁元素对钙离子的测定有影响,所以要预先除去.
(2)溶液中铝离子、铁离子完全转化为氢氧化物沉淀的pH在6左右,加热有利于沉淀聚沉.
(3)茶叶中丰富的有机物来自于植物进行了光合作用.
①称取100g干燥的茶叶,充分灼烧使茶叶灰化,再用研钵磨细后移入烧杯中,然后加入一定量稀盐酸,搅拌、过滤、洗涤.
②向步骤①所得滤液中逐滴加入稀氢氧化钠溶液,调节溶液的pH为6~7左右,再加热煮沸30min,过滤后得到滤液和沉淀.
③向步骤②所得的滤液中加入足量无水碳酸钠,充分搅拌,待充分反应后,过滤、洗涤,得到滤液和沉淀.
请回答下列问题:
(1)步骤①中用到的玻璃仪器是烧杯、漏斗、玻璃棒,灼烧灰化的目的是除去茶叶中的有机物.
(2)实验中用pH试纸测溶液pH值的方法是用洁净的玻璃棒蘸取待测液涂在pH试纸上,与标准比色卡对比读数.
(3)写出步骤②中生成红褐色沉淀的化学方程式3NaOH+FeCl3═Fe(OH)3↓+3NaCl.
(4)计算茶叶中钙元素的含量还需要测定的数据是③中沉淀的质量.
分析 根据过滤操作的仪器解答;根据有机物容易燃烧生成水和二氧化碳等物质;根据测定溶液的pH的方法解答;根据氢氧化钠能与氯化铁反应生成氢氧化铁沉淀和氯化钠解答;根据题意可以判断需要的数据.
解答 解:(1)步骤①是过滤操作,用到的玻璃仪器是烧杯、漏斗、玻璃棒;灼烧灰化的目的是除去茶叶中的有机物.故填:烧杯、漏斗、玻璃棒;除去茶叶中的有机物.
(2)用pH试纸测溶液pH值,可以用洁净的玻璃棒蘸取待测液涂在pH试纸上,与标准比色卡对比读数即可,故填:用洁净的玻璃棒蘸取待测液涂在pH试纸上,与标准比色卡对比读数;
(3)步骤②中生成红褐色沉淀是氢氧化钠与氯化铁反应生成氢氧化铁沉淀和氯化钠,故填:3NaOH+FeCl3═Fe(OH)3↓+3NaCl;
(4)计算茶叶中钙元素的含量需要测定的数据是茶叶质量和③中沉淀的质量,通过碳酸钙的质量可以计算钙元素的质量,再通过茶叶质量(已知)可以计算钙元素质量分数.故填:③中沉淀的质量.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
1.下列实验现象的描述错误的是( )
| A. | 硫在空气中燃烧产生淡蓝色火焰 | |
| B. | 铝和硫酸铜溶液反应,生成黑色的铜 | |
| C. | 铁丝在氧气中剧烈燃烧,火星四射 | |
| D. | 二氧化碳通入紫色石蕊溶液,紫色石蕊溶液变红 |
2.如图是“铁丝在氧气中燃烧”的实验改进装置.下列说法错误的是( )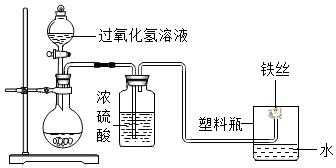

| A. | 氧气无须提前制备和收集 | |
| B. | 用塑料瓶代替集气瓶,实验更安全 | |
| C. | 该装置也可用于二氧化碳和氢气的制备、干燥和检验 | |
| D. | 铁丝在氧气中剧烈燃烧,发出黄色火焰,产生黑色固体 |
9.乙烯(C2H4)气体常温下密度与空气接近,难溶于水,易溶于四氯化铁等有机溶剂.实验室收集乙烯的最佳方法是( )
| A. | 排水法 | B. | 排四氯化碳法 | C. | 向上排空气法 | D. | 向下排空气法 |
13.市场上有“富硒茶叶”、“高钙牛奶”、“铁强化酱油”等商品,这里的“硒、钙、铁”指的是( )
| A. | 单质 | B. | 元素 | C. | 分子 | D. | 原子 |
14.下列化学方程式中符合题意且书写正确的是( )
| A. | 工业上用氢氧化钠溶液除去有害气体SO2:SO2+2NaOH=Na2SO4+H2O | |
| B. | 证明铁能与稀盐酸反应:2Fe+6HCl=2FeCl3+3H2↑ | |
| C. | 正常雨水pH约为5.6的原因:CO2+H2O=H2CO3 | |
| D. | 实验室用熟石灰制烧碱:Ca(OH)2+2NaCl=CaCl2+2NaOH |