题目内容
18.我国古代将炉甘石 (ZnCO3)、赤铜 (Cu2O) 和木炭粉混合后加热到约800℃,得到一种外观似金子的锌和铜的合金(黄铜).(1)黄铜可用来做热交换器,说明黄铜具有良好的导热性;
(2)试写出赤铜(Cu2O) 和木炭粉混合后加热的化学方程式2Cu2O+C$\frac{\underline{\;高温\;}}{\;}$CO2↑+4Cu;
(3)鉴别黄铜和黄金多种方法,用灼烧法鉴别产生的现象及结论是灼烧变黑的为黄铜,无明显现象的是黄金;
(4)用含锌废渣(主要成分为ZnO,杂质为FeO、CuO) 为原料制备七水硫酸锌 (ZnSO4•7H2O) 的流程如图1:

①稀酸A的化学式H2SO4;B的化学式Zn.
②除铁过程中,图2和图3分别表示温度、pH对除铁效果的影响.由图可知除铁时温度应控制在95℃ 为宜,pH应控制在3.2 为宜.
分析 根据给出的转化关系对应的过程分析每个对应的问题,或者直接分析每个问题,从给出的信息中找对应的信息.
解答 解:
(1)黄铜可用来做热交换器,热交换器是能量传递的设备,所以利用的是黄铜具有良好的导热性;
(2)赤铜(Cu2O) 和木炭粉混合后加热,反应物为赤铜和碳,条件是高温,生成的是二氧化碳和铜,对应的化学方程式 2Cu2O+C$\frac{\underline{\;高温\;}}{\;}$CO2↑+4Cu;
(3)鉴别黄铜和黄金多种方法,用灼烧法可以鉴别,是因为在涉及到的金属单质中只有铜能够和氧气在加热的条件下反应生成黑色的氧化铜,所以用灼烧法鉴别是产生的现象及结论是 灼烧变黑的为黄铜,无明显现象的是黄金;
(4)①由于实验的目的是“用含锌废渣(主要成分为ZnO,杂质为FeO、CuO) 为原料制备七水硫酸锌 (ZnSO4•7H2O)”,所以在过程中不能引入硫酸锌之外的杂质,所以加入的酸是硫酸,B物质是能够除去硫酸铜中的铜的锌,所以稀酸A的化学式 H2SO4;B的化学式 Zn.
②除铁过程中,图2和图3分别表示温度、pH对除铁效果的影响.由图可知除铁时温度应控制在 95℃为宜,pH应控制在 3.2 为宜(这两个数据都允许有偏差,但是不能偏差太大).
故答案为:
(1)导热性;
(2)2Cu2O+C$\frac{\underline{\;高温\;}}{\;}$CO2↑+4Cu;
(3)灼烧变黑的为黄铜,无明显现象的是黄金;
(4)①H2SO4; Zn.
②95℃;3.2 (有误差可以,但是偏差不能太大).
点评 读图,从中获得解答题目所需的信息,所以在解答题目时先看解答的问题是什么,然后带着问题去读给出的图进而去寻找解答有用的信息,这样提高了信息扑捉的有效性.解答的问题实际上与复杂的转化图相比,其实很简单很基础,或者可以说转化图提供的是情境,考查基本知识.

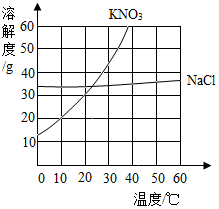 根据给出的KNO3和NaCl两种物质的溶解度表及溶解度曲线,回答问题
根据给出的KNO3和NaCl两种物质的溶解度表及溶解度曲线,回答问题| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解 度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
(2)与KNO3相比较,NaCl的溶解度受温度变化影响较小;
(3)20℃时,在100g水中加入40gKNO3,充分搅拌后,将溶液温度升高到40℃(不考虑水分蒸发),所得溶液是饱和或不饱和中的不饱和溶液.
| A. | 密度比空气大 | B. | 不可燃 | C. | 不支持燃烧 | D. | 常温下是气体 |
| A. | Fe2+:表示1个铁离子带2个正电荷 | B. | $\begin{array}{l}+2\\ Mg\end{array}$:+2价的镁原子 | ||
| C. | 2P:2个磷分子 | D. | O2:氧气 |
| A. | 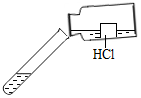 试剂外流 | B. | 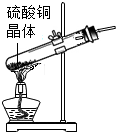 受热仪器破裂 | C. | 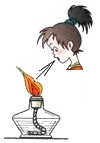 灯内酒精燃烧 | D. |  污染滴管 |
