题目内容
11.根据如图回答问题.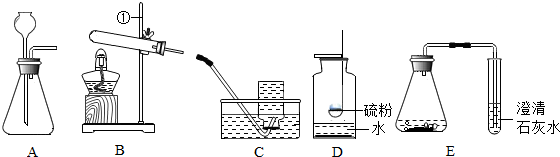
(1)实验室用氯酸钾制取氧气,选用的发生装置是B(填序号),其反应的化学方程式是2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑.
(2)某同学用E装置(气密性良好)在实验室用浓盐酸和石灰石制取二氧化碳及气体的检验,未发现澄清石灰水变浑浊,原因是盐酸浓度太大或澄清石灰水变质等(合理即可).
分析 (1)根据方程式的写法写出用氯酸钾制取氧气的反应原理;根据反应物的状态推出发生装置;
(2)实验制取的二氧化碳气体通入澄清的石灰水中未变浑浊,可以从反应物盐酸是否过浓,使制的二氧化碳中含有HCl气体;或澄清石灰水与空气中的二氧化碳早已反应等进行分析解答.
解答 解:(1)用氯酸钾和二氧化锰制取氧气,反应物是氯酸钾,生成物是氯化钾和氧气,反应条件是二氧化锰做催化剂加热,用最小公倍数法配平即可,氧气后面标上上升符号;反应物的状态是固体和液体制取气体时,反应条件是不需要加热,如果反应物状态是固体与固体反应制取气体时,反应条件需要加热,氯酸钾属于固体所以发生装置选择B;故填:B;2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑;
(2)本实验中用澄清石灰水检验二氧化碳时,发现澄清石灰水未变浑浊,则可能是反应物盐酸过浓,使制的二氧化碳中含有HCl气体或澄清石灰水变质等.
故填:盐酸浓度太大或澄清石灰水变质等(合理即可).
点评 解答本题关键是要熟记实验室用氯酸钾制取氧气的反应原理;了解发生装置的选取方法,熟记二氧化碳的检验方法.

练习册系列答案
相关题目
1.规范操作是化学实验安全、可靠的保证.下列四个实验基本操作中不正确的是( )
| A. | 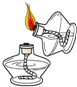 点燃酒精灯 | B. | 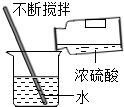 稀释浓硫酸 | C. | 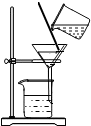 过滤 | D. | 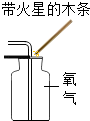 氧气的验满 |
2.下列事实的解释或结论中不正确的是( )
| A. | 金属很难被压缩--是因为金属原子间间隔较小 | |
| B. | 水银温度计受热时水银柱上升--说明汞原子体积变大 | |
| C. | 煤球制成蜂窝煤后燃烧得更旺--是因为增大了煤与空气的接触面积 | |
| D. | 氢气燃烧后的生成物只有水--说明氢气是一种清洁燃料 |
19.为除去粗盐中含有的硫酸钠、氯化镁、氯化钙等杂质,应加入过量的氯化钡、氢氧化钠、碳酸钠等物质.将杂质转化为沉淀过滤除去,再向滤液中加入适量的盐酸得到精盐溶液.该工艺示意如图:
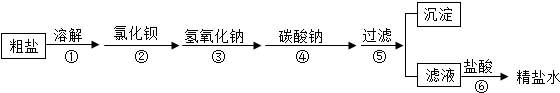
对该过程的认识中,不正确的是( )

对该过程的认识中,不正确的是( )
| A. | 操作③、④两步顺序可以颠倒 | |
| B. | 操作⑤得到的沉淀中有三种成份的物质 | |
| C. | 操作①中需要进行搅拌,目的是加快氯化钠的溶解速率 | |
| D. | 操作⑥中,加入盐酸的目的是除去过量的氢氧化钠和碳酸钠,将滤液的pH调为7 |
20.化学兴趣小组的同学结伴到郊外河畔钓鱼,当他们看到河水浑浊并有异味时非常痛心,他们想用所学的化学知识对河水的水质进行初步探究.
(1)取回水样,在实验室里用过滤的方法将河水变的清澈.
(2)若要测定水样的酸碱度,最适宜选用的是C(填字母序号).
A.紫色石蕊试液 B.无色酚酞溶液 C.pH试纸
(3)他们检测出河水的pH为5,猜想到可能是工厂排放的酸性废水污染了河水,大家经过讨论,想到了要将工厂的酸性废水在不使用指示剂的情况下处理成中性,从下列物质中选择B(填字母序号)最好.
A.废铁 B.石灰石 C.熟石灰 D.生石灰
(4)我们通常把含有较多可溶性钙、镁化合物的水叫硬水,可以用肥皂水来鉴别硬水和软水.
(5)在活动中,某同学不小心被马蜂叮了一下(马蜂的毒液呈酸性),痛痒难耐,用下列物质涂抹可以减轻痛痒的是C(填字母序号).
A.柠檬 B.糖水 C.牙膏 D.牛奶.
(1)取回水样,在实验室里用过滤的方法将河水变的清澈.
(2)若要测定水样的酸碱度,最适宜选用的是C(填字母序号).
A.紫色石蕊试液 B.无色酚酞溶液 C.pH试纸
(3)他们检测出河水的pH为5,猜想到可能是工厂排放的酸性废水污染了河水,大家经过讨论,想到了要将工厂的酸性废水在不使用指示剂的情况下处理成中性,从下列物质中选择B(填字母序号)最好.
A.废铁 B.石灰石 C.熟石灰 D.生石灰
(4)我们通常把含有较多可溶性钙、镁化合物的水叫硬水,可以用肥皂水来鉴别硬水和软水.
(5)在活动中,某同学不小心被马蜂叮了一下(马蜂的毒液呈酸性),痛痒难耐,用下列物质涂抹可以减轻痛痒的是C(填字母序号).
| 柠檬 | 糖水 | 牙膏 | 牛奶 | |
| pH | 2~3 | 7 | 8~9 | 6~7 |
1.分离、除杂和检验是化学实验的重要环节,下列说法不正确的是( )
| A. | 分离CO2、CO混合物时,先用NaOH溶液吸收掉CO2,分离出CO,再向该溶液加足量稀盐酸“释放”出CO2 | |
| B. | 只用一种试剂无法把稀盐酸、BaCl2溶液和KNO3溶液三种溶液区别开 | |
| C. | 要除去CaCl2溶液中混有少量稀盐酸可加入过量的CaCO3充分反应后过滤 | |
| D. | 只用组内溶液相互混合的方法就能将KOH、Na2SO4、CuSO4、MgCl2鉴别出来 |