题目内容
11.肼(N2H4)是氮和氢形成的一种化合物,易溶于水.工业上利用尿素法生产肼,同时得到出副产品十水合碳酸钠,其工艺流程如下:
制肼过程的反应为:CO(NH2)2(尿素)+NaClO+2NaOH═N2H4+Na2CO3+NaCl+H2O.
(1)实验室若配制30%烧碱溶液,所需的玻璃仪器除玻璃棒外,还有BD(填编号).
A.漏斗 B.烧杯 C.烧瓶 D.量筒
(2)已知:Cl2+H2O═HCl+HClO,请推测Cl2与NaOH溶液发生反应的化学方程式:Cl2+2NaOH=NaCl+NaClO+H2O.从后续反应过程来看,若要使原料不浪费,合成次氯酸钠时投入的液氯与烧碱的质量之比为71:160.
(3)在实验室中,欲从母液中分离出十水合碳酸钠晶体.可采用的操作依次为BED(填编号).
A.蒸馏 B.蒸发 C.灼烧 D.过滤 E.冷却结晶
(4)肼具有很好的还原性,且氧化产物无污染,故可用于除去锅炉等设备供水中的溶解氧等.请写出肼除氧时发生反应的化学方程式:N2H4+O2=N2+2H2O.
分析 (1)根据配制溶液需要的玻璃仪器考虑;
(2)根据方程式的书写和相对分子质量的计算考虑;
(3)根据碳酸钠的溶解度随温度变化比较大从溶液中结晶析出的方法:冷却热饱和溶液的方法;
(4)根据方程式的写法考虑.
解答 解:(1)配制溶液需要在烧杯内进行,需要用量筒量取水,用玻璃棒搅拌,还用到胶头滴管,所以选择:BD;
(2)由Cl2+H2O=HCl+HClO,可知Cl2与NaOH溶液发生反应时,氯气先与水反应,生成的盐酸、次氯酸再与氢氧化钠反应生成氯化钠、次氯酸钠和水,所以反应物是氯气和氢氧化钠,生成物是氯化钠、次氯酸钠和水,用观察法配平即可,所以方程式是:Cl2+2NaOH=NaCl+NaClO+H2O;根据氯气和氢氧化钠反应的方程式可知:投入的液氯与烧碱的质量之比为:35.5×2:2×40=71:80,再根据方程式:CO(NH2)2(尿素)+NaClO+2NaOH=N2H4+Na2CO3+NaCl+H2O,可知还需要氢氧化钠两份质量,所以液氯与烧碱的质量之比为71:160;
(3)碳酸钠的溶解度随温度变化比较大从溶液中结晶析出的方法:冷却热饱和溶液的方法,所以先将溶液加热蒸发,再降温,使晶体析出,再进行过滤,所以步骤为:BED;
(4)肼除氧的反应物是肼和氧气,因为氧化产物无污染所以是氢和氧结合成的水,根据质量守恒定律可知生成物还有氮气,再根据观察法配平,所以化学方程式是:N2H4+O2=N2+2H2O.
故答案为:(1)BD;
(2)Cl2+2NaOH=NaCl+NaClO+H2O,160;
(3)BED;
(4)N2H4+O2=N2+2H2O.
点评 解答本题关键是要熟悉方程式的书写注意事项,知道配制溶液需要的仪器,溶质从溶液中结晶析出的方法.

练习册系列答案
相关题目
2.下列实验方案能够达到相应实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 除去氯化亚铁溶液中的氯化铜 | 加入过量的锌粉,过滤 |
| B | 除去铜粉中的铁粉 | 加入过量的稀盐酸,过滤 |
| C | 除去CO2中的CO | 将气体点燃 |
| D | 除去NaCl中的少量Na2CO3 | 溶解、加热浓缩、降温结晶、过滤 |
| A. | A | B. | B | C. | C | D. | D |
6.通过下列实验得出结论,其中正确的是( )
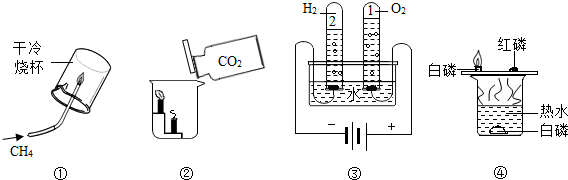
①既可说明甲烷具有可燃性,又说明了甲烷是由氢元素和碳元素组成
②既可说明二氧化碳的密度比空气大,又说明了二氧化碳不能燃烧也不支持燃烧
③说明水是由氢、氧元素组成,又说明了水分子中氢原子和氧原子个数之比为2:1
④既可探究可燃物的燃烧条件,又说明了白磷的着火点比红磷低.

①既可说明甲烷具有可燃性,又说明了甲烷是由氢元素和碳元素组成
②既可说明二氧化碳的密度比空气大,又说明了二氧化碳不能燃烧也不支持燃烧
③说明水是由氢、氧元素组成,又说明了水分子中氢原子和氧原子个数之比为2:1
④既可探究可燃物的燃烧条件,又说明了白磷的着火点比红磷低.
| A. | ①②③ | B. | ①③④ | C. | ②③④ | D. | ①②④ |
16.下列金属中,最不易和空气中的空气发生反应的是( )
| A. | Zn | B. | Cu | C. | Fe | D. | Mg |
3.在20℃时,100g水中最多可溶解A物质50g;在60℃时,100g水中最多可溶解B物质100g,则A、B 两种物质的溶解度大小比较为( )
| A. | 无法比较 | B. | A=B | C. | A<B | D. | A>B |
20.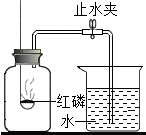 如图所示装置可用来测定空气中氧气的含量.下列说法中不正确的是( )
如图所示装置可用来测定空气中氧气的含量.下列说法中不正确的是( )
 如图所示装置可用来测定空气中氧气的含量.下列说法中不正确的是( )
如图所示装置可用来测定空气中氧气的含量.下列说法中不正确的是( )| A. | 实验时红磷要过量 | |
| B. | 可用木炭替代红磷进行实验 | |
| C. | 要等到充分冷却后才能打开止水夹 | |
| D. | 该实验证明空气中氧气的含量约占$\frac{1}{5}$体积. |
1.酸菜腌制过程中产生的亚硝酸钠食用后对人身体有害.亚硝酸钠(NaNO2)中氮元素的化合价为( )
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
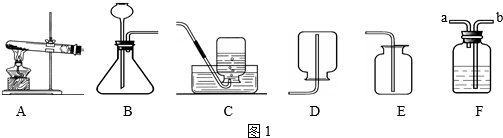
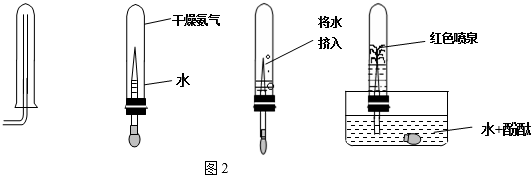
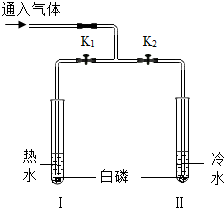 依据如图装置进行实验.
依据如图装置进行实验.