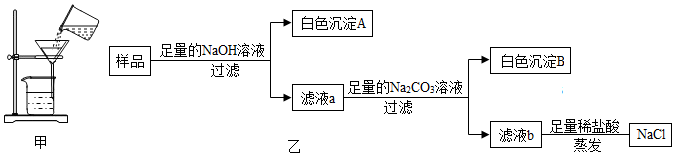
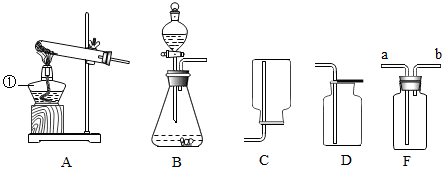
题目内容
19.如图所示是A、B、C三种固体物质的溶解度随温度变化的曲线,根据图示回答: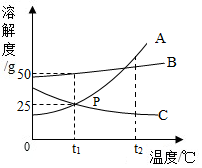
(1)影响固体物质溶解的主要因素有①③④⑤(填序号)
①温度 ②压强 ③溶剂质量 ④溶剂性质 ⑤溶质性质
(2)t2℃时,A、B、C三种物质的溶解度分别用abc表示,则它们的大小关系是a>b>c(用“<”或“>”或“=”连接)
(3)t1℃时,B物质饱和溶液的溶质质量分数是33.3%;
(4)t2℃时,将等质量的A、B、C三种物质的饱和溶液同时降温至t1℃,所得溶液中溶质质量分数最小的是C,析出晶体质量最大的是A.
(5)实验室需要135g20%的C溶液,配制该溶液需要控制的温度范围是小于t1℃时.
(6)固体A中混有的少量的C杂质,若要得到较纯净的A物质,有以下两种方法:甲同学采用的提纯方法主要步骤是:将固体配成饱和溶液降温结晶,过滤,洗涤滤渣等.
乙同学采用的提纯方法主要步骤是:将固体配成饱和溶液升温结晶,过滤,蒸发滤液.
丙同学认为,乙同学的方法不合理,原因是乙同学无法将c完全除去,所得溶液为a、c的混合溶液,蒸干后,所得固体仍为混合物.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)影响固体物质溶解的主要因素有:温度、溶剂质量、溶剂性质、溶质性质,故选:①③④⑤;
(2)通过分析溶解度曲线可知,t2℃时,A、B、C三种物质的溶解度分别用abc表示,则它们的大小关系是:a>b>c;
(3)t1℃时,B物质的溶解度是50g,所以B物质饱和溶液的溶质质量分数是:$\frac{50g}{150g}$×100%=33.3%;
(4)t1℃时,B物质的溶解度最大,A、C物质的溶解度相等,降低温度,A、B会析出晶体,C不会析出晶体,应该按照t2℃时的溶解度计算,所以所得溶液中溶质质量分数最小的是C,A物质的溶解度从t2℃到t1℃,变化最大,所以析出晶体质量最大的是A;
(5)C物质在t1℃时的溶解度是25g,饱和溶液的质量分数为:$\frac{25g}{125g}$×100%=20%,所以实验室需要135g20%的C溶液,配制该溶液需要控制的温度范围是:小于t1℃时;
(6)a物质的溶解度受温度的影响较大,c物质的溶解度随温度的升高而减小,所以乙同学无法将c完全除去,所得溶液为a、c的混合溶液,蒸干后,所得固体仍为混合物.
故答案为:(1)①③④⑤;
(2)a>b>c;
(3)33.3%;
(4)C,A;
(5)小于t1℃时;
(6)乙同学无法将c完全除去,所得溶液为a、c的混合溶液,蒸干后,所得固体仍为混合物.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

| A. | 木炭在氧气中剧烈燃烧,发出白光,生成的气体使澄清石灰水变浑浊 | |
| B. | 硫粉在氧气中燃烧更旺,火焰呈蓝紫色,生成有刺激性气味的气体 | |
| C. | 红磷在空气中燃烧,产生大量的白烟 | |
| D. | 铁在氧气中剧烈燃烧,火星四射,生成四氧化三铁 |

| A. | 向生铁中加入稀硫酸 | |
| B. | 向稀盐酸中加入水 | |
| C. | 等质量的镁片和铝片分别加入足量稀盐酸反应 | |
| D. | 电解水实验正负极的气体质量随时间的变化 |
①浓硫酸 ②浓盐酸 ③苛性钠 ④食盐 ⑤生石灰 ⑥稀硫酸.
| A. | ③⑤ | B. | ①⑥ | C. | ①⑤ | D. | ②④ |
| A. | 分子的体积很小 | B. | 分子间有间隔 | ||
| C. | 不同分子的化学性质不同 | D. | 分子在不断运动 |
| A. | 可燃物只要与氧气接触就能燃烧 | |
| B. | 档案失火,用泡沫灭火器灭火 | |
| C. | 用水灭火是为了使可燃物的温度降到着火点以下 | |
| D. | 为扑灭森林火灾而设置隔离带,是为了隔绝氧气 |
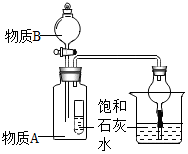 化学小组的同学利用如图所示装置进行实验.集气瓶中装有纯净物A,分液漏斗中盛有物质B.
化学小组的同学利用如图所示装置进行实验.集气瓶中装有纯净物A,分液漏斗中盛有物质B.