题目内容
氯酸钾和二氧化锰混合物共5.7克进行加热,完全反应后剩余固体的质量为3.78g,问:
(1)生成的氧气的质量为 .
(2)原混合物中氯酸钾有多少克?
(1)生成的氧气的质量为
(2)原混合物中氯酸钾有多少克?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:(1)依据质量守恒定律反应前后固体的质量之差即为反应中生成的氧气质量;
(2)利用氧气的质量结合方程式即可求出氯酸钾的质量;
(2)利用氧气的质量结合方程式即可求出氯酸钾的质量;
解答:解:(1)根据质量守恒定律,生成氧气的质量=5.7g-3.78g=1.92g
(2)设原混合物中氯酸钾的质量至少为x,
2KClO3
2KCl+3O2↑
245 96
x 1.92g
=
x=4.9g
故答案为:(1)1.92g;(2)原混合物中氯酸钾的质量为4.9g.
(2)设原混合物中氯酸钾的质量至少为x,
2KClO3
| ||
| △ |
245 96
x 1.92g
| 245 |
| x |
| 96 |
| 1.92g |
x=4.9g
故答案为:(1)1.92g;(2)原混合物中氯酸钾的质量为4.9g.
点评:此题是化学方程式的计算考查题,解题的关键是根据质量守恒定律,由反应前后固体物质质量差即反应所产生氧气的质量;

练习册系列答案
 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案
相关题目
乙醇(用X表示)完全燃烧的化学方程式为X+3O2═2CO2+3H2O试推断乙醇的化学式是( )
| A、C3H8 |
| B、C2H6 |
| C、C2H6O |
| D、C4H6O2 |
 构建知识网络是一种重要的学习方法.如图是小冰学习了稀盐酸的化学性质后画出的知识网络图,“-”表示相连的两种物质能发生反应,A、B、C属于不同类别的化合物.
构建知识网络是一种重要的学习方法.如图是小冰学习了稀盐酸的化学性质后画出的知识网络图,“-”表示相连的两种物质能发生反应,A、B、C属于不同类别的化合物.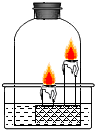 如图所示:水槽内盛有澄清石灰水,点燃高低两支蜡烛,用钟罩将其扣在水槽内.实验可以观察到的现象是什么?
如图所示:水槽内盛有澄清石灰水,点燃高低两支蜡烛,用钟罩将其扣在水槽内.实验可以观察到的现象是什么? 早在春秋战国时期,我国就开始生产和使用铁器.工业上炼铁的原理是利用一氧化碳和氧化铁的反应.某化学兴趣小组利用如图装置进行实验探究,
早在春秋战国时期,我国就开始生产和使用铁器.工业上炼铁的原理是利用一氧化碳和氧化铁的反应.某化学兴趣小组利用如图装置进行实验探究,