题目内容
6.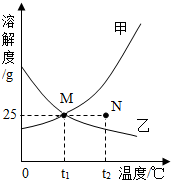 如图为甲、乙两种固体物质在水中的溶解度曲线.请回答下列问题:
如图为甲、乙两种固体物质在水中的溶解度曲线.请回答下列问题:(1)在t1℃时,M点表示甲、乙两固体物质的溶解度是25g;
(2)固体甲物质的溶解度随温度的升高而增大;
(3)在t2℃时,处在N点的甲溶液属于不饱和(填“饱和”或“不饱和”)溶液.
(4)在t1℃时,100g的水最多能溶解乙物质25g.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度曲线可知,在t1℃时,M点表示甲、乙两固体物质的溶解度是25g;
(2)固体甲物质的溶解度随温度的升高而增大;
(3)在t2℃时,处在N点的甲溶液在溶解度曲线的下面,属于不饱和溶液;
(4)在t1℃时,乙物质的溶解度是25g,所以100g的水最多能溶解乙物质25g.
故答案为:(1)25;
(2)增大;
(3)不饱和;
(4)25.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
17.质量守恒定律也有人称之为“物质不灭定律”,对于在化学反应中“物质不灭”的理解正确的组合是( )
①构成物质的分子种类不变 ②构成物质的元素种类不变
③构成物质的原子种类不变 ④物质的种类和质量不变.
①构成物质的分子种类不变 ②构成物质的元素种类不变
③构成物质的原子种类不变 ④物质的种类和质量不变.
| A. | ①② | B. | ②③ | C. | ①③ | D. | ②④ |
14.下列食品①玉米 ②花生 ③草鱼 ④大米中富含糖类的是( )
| A. | ①③ | B. | ①④ | C. | ②④ | D. | ①② |
1.下列能源属于不可再生的是( )
| A. | 煤 | B. | 风能 | C. | 氢能 | D. | 水能 |
11.下列实验现象的描述正确的是( )
| A. | 蜡烛在空气中燃烧生成二氧化碳和水 | |
| B. | 硫在空气中燃烧,发出明亮的蓝紫色火焰 | |
| C. | 铁丝在氧气中燃烧,火星四射,生成黑色固体,放出大量的热 | |
| D. | 木炭在氧气中燃烧,发出黄色火焰,生成有刺激性气味的气体 |
18.高铁酸钠(Na2FeO4)是一种性能优良的净水剂,除了用于饮用水消毒、净化外,还用于污水处理,下列说法正确的是( )
| A. | 高铁酸钠中含有7个原子 | |
| B. | 高铁酸钠中铁元素的质量分数为40% | |
| C. | 高铁酸钠是由三种元素组成的化合物 | |
| D. | 高铁酸钠中铁、氧元素的质量比为1:4 |
15.运载火箭的燃料是偏二甲肼(C2H8N2).有关偏二甲肼的叙述中,正确的是( )
| A. | 偏二甲肼中含有氮气 | |
| B. | 偏二甲肼的相对分子质量是60g | |
| C. | 偏二甲肼由碳、氢、氮三种元素组成 | |
| D. | 偏二甲肼中碳、氢、氮的质量比为1:4:1 |