题目内容
某纯碱样品中含 有少量氯化钠,取该样品11g,全部溶液在100g水中,再逐渐滴加氯化钙溶液
有少量氯化钠,取该样品11g,全部溶液在100g水中,再逐渐滴加氯化钙溶液 ,反应的情况如图所示,A点时,过滤,得到滤液242g,计算:
,反应的情况如图所示,A点时,过滤,得到滤液242g,计算:
(1)反应生成沉淀的质量m为 g.
(2)滤液中溶质的质量分数.

解:(1)反应生成沉淀的质量为:11g+100g+141g﹣242g=10g,
故填:10.
(2)设碳酸钠的质量为x,生成氯化钠的质量为y,
Na2CO3+CaCl2═CaCO3↓+2NaCl,
106 100 117
x 10g y
 =
= =
=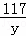 ,
,
x=10.6g,y=11.7g,
滤液中溶质的质量分数为: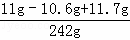 ×100%=5%,
×100%=5%,
 答:滤液中溶质的质量分数为:
答:滤液中溶质的质量分数为: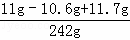 ×100%=5%.
×100%=5%.

下列实验操作和结论的说法正确的是( )
|
| A. | 取少量溶液于试管中,滴加BaCl2,有白色沉淀生成,证明溶液中一定含有Ag+ |
|
| B. | 向某固体中滴加稀盐酸,有气泡产生,则该固体一定是碳酸盐 |
|
| C. | 只用水就可以将NH4NO3、BaSO4、CaO、NaOH四种固体物质区别出来 |
|
| D. | 把燃着的木条插入某瓶无色气体中,木条熄灭,证明瓶中的气体一定是二氧化碳 |
咸宁城际铁路的建成将进一步推动我市经济的发展,在修建铁路的土石方爆破中要用到黑火药,黑火药爆炸时发生反应的化学方程式是2KNO3+3C+S K2S+3CO2↑+X↑,根据以上信息,下列说法错误的是( )
K2S+3CO2↑+X↑,根据以上信息,下列说法错误的是( )
|
| A. | X的化学式是N2 |
|
| B. | 黑火药在混合物 |
|
| C. | KNO3中氨元素的化合价为+5价 |
|
| D. | KNO3属于氨肥 |
将一定质量金属M的粉末放入盛有Cu(NO3)2溶液的烧杯中,充分反应后溶液呈无色;继续向烧杯中加入一定量的AgNO3溶液,待充分反应后过滤,得蓝色滤液和滤渣.根据实验分析,以下结论错误的是( )
| A. | 金属活动性顺序:M>Cu>Ag |
| B | 滤液中一定含有M的阳离子和Cu2+ |
| C. | 滤渣中一定含有Ag和Cu |
| D. | 向滤液中滴加稀盐酸,可能产生白色沉淀 |
如图所示是两种气体发生化学反应的微观示意图,其中相同的球代表同种原子,下列说法正确的是( )

|
| A. | 化学反应前后原子的种类不变 |
|
| B. | 生成物一定是氧化物 |
|
| C. | 化学反应前后分子的种类不变 |
|
| D. | 该反应属于置换反应 |
