题目内容
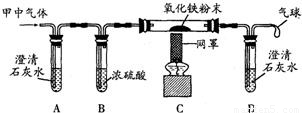
已知在CO和CO2的混合气体中,氧元素的质量分数为60%,将12g该混合气体通过足量灼热的氧化铜粉末,充分反应后CO全部转化为CO2(化学方程式CO+CuO![]() Cu+CO2)再将所得气体全部通入足量的澄清石灰水(化学方程式CO2+Ca(OH)2=CaCO3↓+H2O),可得沉淀多少克?
Cu+CO2)再将所得气体全部通入足量的澄清石灰水(化学方程式CO2+Ca(OH)2=CaCO3↓+H2O),可得沉淀多少克?
答案:
解析:
提示:
解析:
|
发生反应的化学方程式为: CO+CuO CO2+Ca(OH)2=CaCO3↓+H2O 根据反应可知,CO与灼热氧化铜反应,转化成CO2,所有的CO2通入足量澄清石灰水中,转化为CaCO3沉淀.混合气体中的碳元素全部转化到碳酸钙中. 设碳酸钙的质量为x 有 C ~ CaCO3 12 100 12g×(1-60%) x 答:可得沉淀40g. |
提示:
|
考查同学灵活运用质量守恒思想解题的能力. |

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
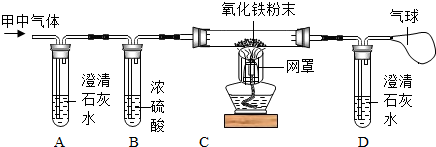
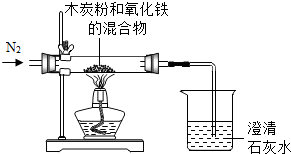 (2012?黄冈模拟)已知木炭粉(假设木炭粉中不含其他杂质)和Fe2O3,在加热条件下发生化学反应,兴趣小组同学对该实验进行如下探究.
(2012?黄冈模拟)已知木炭粉(假设木炭粉中不含其他杂质)和Fe2O3,在加热条件下发生化学反应,兴趣小组同学对该实验进行如下探究.