题目内容
1.将一定量的苯(化学式为C6H6,相对分子质量为78)在有限量的空气中快速不完全燃烧,产生大量的黑烟,得到碳、一氧化碳、二氧化碳和水的总质量为19g,没有其他生成物.4种生成物中水为5.4g,固态的碳为3.6g.则上述过程中产生的一氧化碳的质量为( )| A. | 2.8g | B. | 5.6g | C. | 11.2g | D. | 1.4g |
分析 根据题目中的信息“得到碳、一氧化碳、二氧化碳和水的总质量为19g,没有其他生成物.4种生成物中水为5.4g,固态的碳为3.6g”,则可知一氧化碳、二氧化碳的总质量为19g-5.4g-3.6g=10g;根据“生成物中水为5.4g”,可求氢元素的质量,根据氢元素的质量可求苯的质量,则可得碳元素的质量,再根据质量守恒定律分析,各元素的质量在反应前后不变,然后推算一氧化碳的质量.
解答 解:
根据题目中的信息“得到碳、一氧化碳、二氧化碳和水的总质量为19g,没有其他生成物.4种生成物中水为5.4g,固态的碳为3.6g”,则可知一氧化碳、二氧化碳的总质量为19g-5.4g-3.6g=10g;根据“生成物中水为5.4g”,可求氢元素的质量为$5.4g×\frac{2}{1×2+16}×100%$=0.6g,根据氢元素的质量可求苯的质量为0.6g÷$\frac{1×6}{78}×100%$=7.2g,则再根据质量守恒定律分析,各元素的质量在反应前后不变,然后可得一氧化碳、二氧化碳的中碳元素的质量为7.2g-3.6g=3.6g.
设一氧化碳的质量为x,则二氧化碳的质量为10g-x,则x×$\frac{12}{12+16}×100%$+(10g-x)×$\frac{12}{12+16×2}×100%$=3.6g.解得x=5.6g.
故选B.
点评 本题考查化学反应方程式的计算,为基础性习题,把握水的质量及CO、CO的质量、守恒法计算为解答的关键,侧重分析与计算能力的考查,题目难度较大.

练习册系列答案
 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
11.下列生产生活中发生的变化属于化学变化的是( )
| A. |  石油分馏 | B. |  灯泡通电发光 | ||
| C. |  湿衣服晾干 | D. |  淀粉转化成葡萄糖 |
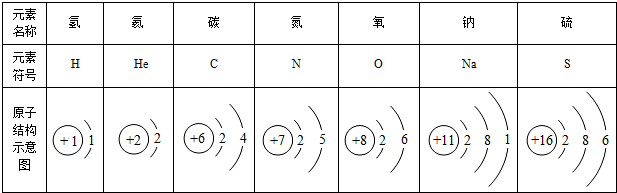
12.随着日本福岛核电站放射性碘泄漏,碘这种元素被人们所认知.如图是元素周期表中提供的碘元素的部分信息及碘原子的结构示意图.下列说法错误的是( )


| A. | 碘的相对原子质量为126.9,原子核内质子数为53 | |
| B. | 碘原子核外共有53个电子,最外层有7个电子 | |
| C. | 碘元素属于非金属元素,能形成碘分子I2 | |
| D. | 碘原子核内的中子数也为53 |
6.下列除去杂质(括号内为杂质)的方法不正确的是( )
| A. | Cu(Fe):可将混合粉末加入到足量硫酸铜溶液中,充分反应后过滤 | |
| B. | FeCl2(CuCl2):可往混合液中加入过量铁粉、充分反应后过滤 | |
| C. | CO(CO2):可将混合气体通过盛有足量澄清石灰水溶液的洗气瓶 | |
| D. | NaCl(Na2CO3):可往混合液中加入适量Ca(OH)2溶液,完全反应后过滤 |
14.下列物质中含有氢分子的是( )
| A. | 硫酸 | |
| B. | 液氢 | |
| C. | 氯酸钾与二氧化锰混合加热后生成的气体 | |
| D. | 蒸馏水 |
15.水是生命之源,下列关于水的叙述中正确的是( )
| A. | 用滤纸过滤可以降低水的硬度 | |
| B. | 用肥皂水可以区分硬水和软水 | |
| C. | 为了保护水资源,禁止使用化肥和农药 | |
| D. | 电解水时,负极端的玻璃管中产生的气体能使带火星的木条复燃 |
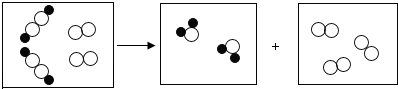
 与
与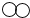 的质量比为(m+2):m.
的质量比为(m+2):m.