题目内容
19.某同学在实验室进行有关浓硫酸的实验,观察到瓶上的标签如表所示.他从瓶中倒出100毫升用于配制稀硫酸.求:(1)这100毫升浓硫酸的质量是184克,其中含溶质硫酸180.32克.
(2)欲配制1000克质量分数为19.6%的稀硫酸,需要多少毫升这种浓硫酸和多少克水?
| 浓硫酸(H2SO4)500毫升 | |
| 浓度(质量分数) | 98% |
| 密度 | 1.84克/厘米3 |
| 相对分子质量 | 98 |
| 强腐蚀性,阴冷,密封贮藏 | |
分析 溶质质量=溶液质量×溶质质量分数;
溶液稀释前后,溶质质量不变.
解答 解:(1)这100毫升浓硫酸的质量是1.84g/mL×100mL=184g,其中含溶质硫酸质量为:184g×98%=180.32g,
故填:184;180.32.
(2)设需要浓硫酸体积为x,
根据题意有:x×1.84g/mL×98%=1000g×19.6%,
x=108.7mL,
需要水的质量为:1000g-108.7mL×1.84g/mL=800g,
答:欲配制1000克质量分数为19.6%的稀硫酸,需要108.7mL这种浓硫酸和200g水.
点评 本题主要考查溶液质量、溶质质量分数之间的关系,比较简单.

练习册系列答案
相关题目
14.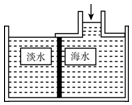 海水淡化可采用膜分离技术.如右图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入淡水池,而海水中的各种溶质不能通过淡化膜,从而得到淡水.对加压后右侧海水成分进行分析,错误的是( )
海水淡化可采用膜分离技术.如右图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入淡水池,而海水中的各种溶质不能通过淡化膜,从而得到淡水.对加压后右侧海水成分进行分析,错误的是( )
 海水淡化可采用膜分离技术.如右图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入淡水池,而海水中的各种溶质不能通过淡化膜,从而得到淡水.对加压后右侧海水成分进行分析,错误的是( )
海水淡化可采用膜分离技术.如右图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入淡水池,而海水中的各种溶质不能通过淡化膜,从而得到淡水.对加压后右侧海水成分进行分析,错误的是( )| A. | 海水的溶质质量分数不变 | B. | 溶剂质量减少 | ||
| C. | 海水质量减少 | D. | 溶质质量不变 |
4.打开汽水瓶盖,会逸出大量气泡,根据汽水中二氧化碳的溶解情况分析,下列说法中错误的是( )
| A. | 溶质减少 | B. | 溶解度减小 | ||
| C. | 浓度减小 | D. | 饱和溶液变成不饱和溶液 |
11.下列关于溶液、溶解度的说法中,错误的是( )
| A. | 不饱和溶液转化为饱和溶液,溶液中溶质的质量分数可能保持不变 | |
| B. | 温度降低时,原饱和溶液可能不析出晶体 | |
| C. | 温度一定时,硝酸钾的溶解度及硝酸钾的饱和溶液中溶质的质量分数各有一定值 | |
| D. | 某溶液析出晶体后,溶液中溶质的质量分数一定减小 |
8.下列各组物质,不加其他试剂就能一一鉴别出来的是( )
| A. | Ba(NO3)2、NaOH、H2SO4、KCl | B. | AgNO3、KCl、HNO3、MgCl2 | ||
| C. | Ba(NO3)2、NaCl、CuSO4、NaOH | D. | FeCl3、KOH、NaCl、NaNO3 |
9.实验室中的下列物质需要密封保存的是( )
| A. | 氯化钠 | B. | 大理石 | C. | 浓盐酸 | D. | 木炭 |
 金丽温高速铁路于2016年1月10日正式通车营运,标志着丽水进入了高铁时代,高速铁路铺设的是无缝钢轨,钢铁的主要成分是铁,铁有多种氧化物,请回答:
金丽温高速铁路于2016年1月10日正式通车营运,标志着丽水进入了高铁时代,高速铁路铺设的是无缝钢轨,钢铁的主要成分是铁,铁有多种氧化物,请回答: