题目内容
11.下列叙述中,正确的是( )| A. | 12g碳所含的原子数就是阿伏加德罗常数 | |
| B. | 阿伏加德罗常数没有单位 | |
| C. | “物质的量”指物质的质量 | |
| D. | 摩尔是表示物质的量的单位,每摩尔物质含有阿伏加德罗常数个微粒 |
分析 碳的摩尔质量是12g/mol;
阿伏加德罗常数的单位是$\frac{1}{mol}$;
“物质的量”不是指物质的质量,但是它们之间有一定的联系;
摩尔是表示物质的量的单位,每摩尔物质不一定含有阿伏加德罗常数个微粒.
解答 解:A、碳的摩尔质量是12g/mol,因此12g碳所含的原子数就是阿伏加德罗常数,该选项说法正确;
B、阿伏加德罗常数的单位是$\frac{1}{mol}$,该选项说法不正确;
C、“物质的量”不是指物质的质量,该选项说法不正确;
D、摩尔是表示物质的量的单位,每摩尔物质不一定含有阿伏加德罗常数个微粒,例如1mol氢气中含有的氢原子数是阿伏加德罗常数个微粒的2倍,该选项说法不正确.
故选:A.
点评 解答时要注意区分物质的量、阿伏伽德罗常数、摩尔质量之间的关系,只有充分了解这些概念的含义,才能够正确的分析、解决问题.

练习册系列答案
相关题目
1.据媒体报道,不法菜贩在白菜上喷洒甲醛(化学式CH2O)溶液进行保鲜.甲醛是无色、具有刺激性气味的有毒物质.下列说法不正确的是( )
| A. | 甲醛分子中含有氢原子 | |
| B. | 甲醛是由三种元素组成的 | |
| C. | 甲醛中碳元素的质量分数为80% | |
| D. | 甲醛分子中碳、氢、氧的原子个数比是1:2:1 |
2.某校化学课外活动小组在一次活动中,取刚降到地面的雨水水样,每隔5分钟用pH计测定一次pH,其数据如表:
已知:正常雨水的pH约为5.6,酸雨的pH小于5.6.
(1)所取的雨水是否为酸雨?是(填“是”或“否”);在测定的期间,雨水水样的酸性随着时间的变化逐渐增强(填“增强”或“减弱”).
(2)经调查,这一地区有一座燃煤发电厂(生产过程中产生SO2),某同学设计用火碱来吸收生产过程中产生的SO2,将其转化成亚硫酸钠(Na2SO3).请你帮他写出该反应的化学方程式:SO2+2NaOH═Na2SO3+H2O.
(3)若用pH试纸测定雨水的酸碱度,测定方法是:将PH试纸放在玻璃板上,用干净的玻璃棒蘸取少量待测雨水,显色后对照比色卡,读出PH值.
| 测定时刻 | 6:05 | 6:10 | 6:15 | 6:20 | 6:25 | 6:30 |
| p H | 4.95 | 4.94 | 4.94 | 4.88 | 4.86 | 4.85 |
(1)所取的雨水是否为酸雨?是(填“是”或“否”);在测定的期间,雨水水样的酸性随着时间的变化逐渐增强(填“增强”或“减弱”).
(2)经调查,这一地区有一座燃煤发电厂(生产过程中产生SO2),某同学设计用火碱来吸收生产过程中产生的SO2,将其转化成亚硫酸钠(Na2SO3).请你帮他写出该反应的化学方程式:SO2+2NaOH═Na2SO3+H2O.
(3)若用pH试纸测定雨水的酸碱度,测定方法是:将PH试纸放在玻璃板上,用干净的玻璃棒蘸取少量待测雨水,显色后对照比色卡,读出PH值.
19.下列变化中属于缓慢氧化的是( )
| A. | 沼气的燃烧 | B. | 电灯的发光放热 | C. | 种植物的呼吸 | D. | 蜡烛的融化 |
6.下面是对四个实验绘制的图形,其中实验结果与图形对应准确的是( )
| A. | 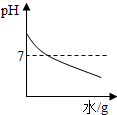 是pH=13的NaOH溶液中加水稀释 是pH=13的NaOH溶液中加水稀释 | |
| B. | 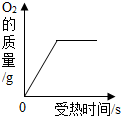 是用适量的KClO3和MnO2混合物加热制O2 是用适量的KClO3和MnO2混合物加热制O2 | |
| C. |  是向一定量的稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量 是向一定量的稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量 | |
| D. | 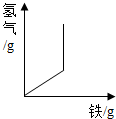 向一定质量的稀盐酸中加入铁粉至过量 向一定质量的稀盐酸中加入铁粉至过量 |
16.已知氨水的密度小于1,质量分数为25.0%的氨水与质量分数为45.0%的氨水等体积混合后,所得溶液的质量分数为( )
| A. | 等于35% | B. | 大于35% | C. | 小于35% | D. | 无法确定 |

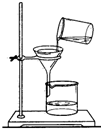 小明同学将浑浊的河水样品倒入烧杯中,先加入明矾粉未搅拌溶解,静置一会儿后,采用如图所示装置进行过滤,请问:
小明同学将浑浊的河水样品倒入烧杯中,先加入明矾粉未搅拌溶解,静置一会儿后,采用如图所示装置进行过滤,请问: