题目内容
15.某同学测石膏(CuSO4•2H2O)中的结晶水含量,测得实验数据如下:| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 | 测得晶体中结晶水的含量 |
| 11.7g | 22.7g | 20.7g |
(2)表中实际测得的结晶水的含量是18.1%.
分析 (1)根据石膏(CuSO4•2H2O)的化学式求出结晶水含量;
(2)根据反应前后的固体质量的差来计算水的质量;根据硫酸铜晶体的质量和生成结晶水的质量进行计算;
解答 解:
(1)石膏(CuSO4•2H2O)中结晶水含量的理论值是$\frac{2×18}{160+2×18}×$100%≈18.3%;
(2)由表格中的数据,水的质量为反应前后固体质量的差,则水的质量为22.7g-20.7g=2g;硫酸铜晶体中结晶水的质量分数为:$\frac{2g}{22.7g-11.7g}×$100%≈18.1%;
答案:
(1)18.3%;
(2)18.1%
点评 本题考查学生利用试验数据来分析数据并应用数据进行计算,较好的训练了学生对实验数据的分析应用能力,并应熟悉化学方程式及溶质质量分数的计算来解答.

练习册系列答案
相关题目
5.下列能源中属于可再生能源的是( )
| A. | 煤 | B. | 石油 | C. | 酒精 | D. | 天然气 |
3.下列实验现象的描述正确的是( )
| A. | 将光亮的铜丝插入稀盐酸中,有气泡产生 | |
| B. | 硫在空气中燃烧,发出明亮的蓝紫色火焰,生成无色无味的气体 | |
| C. | 铁丝在空气中点燃,剧烈燃烧,火星四射,生成黑色固体 | |
| D. | 将人体呼出的气体导入紫色石蕊试液,试液变成红色 |
10.下列各组物质能够在pH=1的溶液中大量共存,且为无色透明溶液的是( )
| A. | Mg(NO3)2、CuSO4、NaCl | B. | K2SO4、NaNO3、NH4Cl | ||
| C. | CaCl2、Na2CO3、AgNO3 | D. | BaCl2、Na2SO4、NaOH |
20.某碳酸钙和氧化钙组成的混合物中钙元素的质量分数为60%,将100g该混合物高温煅烧至固体质量不再改变.有关结论正确的是( )
| A. | 锻烧后固体中钙元素的质量分数减少 | |
| B. | 共生成84g氧化钙 | |
| C. | 锻烧后固体中氧元素的质量不变 | |
| D. | 共生成16g二氧化碳 |
4.化学开始成为一门独立的自然学科的基础是( )
| A. | 火的发现和利用 | |
| B. | 原子论和分子学说的创立 | |
| C. | 门捷列夫发现元素周期表 | |
| D. | 发现和合成的新物质已超过7000万种 |
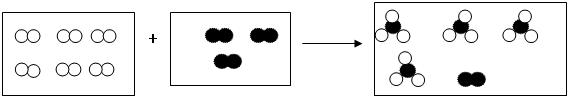
 ”和“
”和“ ”分别代表两种不同的单质的分子A2和B2,它们在一定条件下能发生化学反应,其反应的微观示意图如图:
”分别代表两种不同的单质的分子A2和B2,它们在一定条件下能发生化学反应,其反应的微观示意图如图: