题目内容
2.在金属活动顺序里,金属的位置越靠前,它的活动性就越越强;银与稀盐酸不能发生反应;铝与硝酸银溶液能发生反应;写出最活泼金属的元素符号K.分析 根据金属活动性顺序的意义进行分析,在金属活动性顺序中,金属的位置越靠前,它的活动性越强,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,利用这些知识结合类比的方法可解决此题.
解答 解:在金属活动性顺序中,金属的位置越靠前,它的活动性越强;位于氢前面的金属能置换出盐酸、稀硫酸中的氢;银位于H后面与稀盐酸不发生反应;位于前面的金属能把位于后面的金属从它们的盐溶液里置换出来,铝位于银前与硝酸银溶液能发生反应;最活泼金属为钾.
故答案为:越强;不能;能;K.
点评 本题考查了金属活动性顺序的意义,完成此题,可以依据已有的知识进行,同时也要求同学们要加强基础知识的储备,以便能灵活应用.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
13.下列词语中,一定包含有化学变化的是( )
| A. | 花香四溢 | B. | 蜡炬成灰 | C. | 滴水成冰 | D. | 木已成舟 |
10.下列物质属于纯净物的是( )
| A. | 河水 | B. | 清新空气 | C. | 液态汞 | D. | 糖水(溶液) |
17.下列溶液混合不能发生复分解反应的是( )
| A. | Na2CO3和CaCl2 | B. | NaOH和KCl | C. | KOH和HCl | D. | K2CO3 和HCl |
14.下列关于实验室里使用药品时需要注意的事项中,不正确的是( )
| A. | 块状药品可以用手拿 | |
| B. | 不能把鼻孔凑到容器口去闻药品气味 | |
| C. | 特别注意不得尝药品的味道 | |
| D. | 用剩的药品不要放回原瓶 |
 和
和 分别表示两种不同的原子,请根据条件填写答案.
分别表示两种不同的原子,请根据条件填写答案.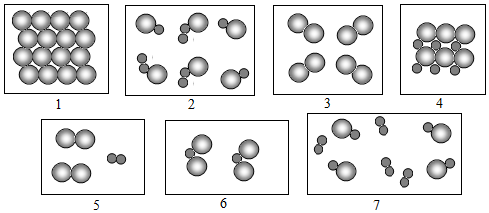
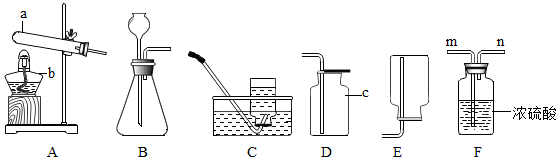
 某同学对蜡烛的性质进行如下探究.
某同学对蜡烛的性质进行如下探究.