题目内容
4.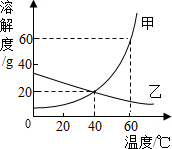 如图所示,甲、乙是两种物质的溶解度曲线,下列叙述不正确的是( )
如图所示,甲、乙是两种物质的溶解度曲线,下列叙述不正确的是( )| A. | 20℃时甲的溶解度大于乙的溶解度 | |
| B. | 60℃时,在100g水中加入100g甲,充分溶解后溶液的质量是200g | |
| C. | 40℃时,甲、乙两种物质饱和溶液中溶质的质量相等 | |
| D. | 采用升温的方法可将乙的不饱和溶液转化为饱和溶液 |
分析 根据固体物质的溶解度曲线堵塞意义分析:①比较不同物质在同一温度下的溶解度的大小;②查出某物质在一定温度时的溶解度,根据溶解度进行有关分析与计算,③判断出物质的溶解度随温度变化的变化情况,从而确定饱和溶液和不饱和溶液的转化方法.
解答 解:A、通过分析溶解度曲线可知,20℃时,甲的溶解度大于乙的溶解度,故A正确;
B、60℃时,甲的溶解度是60g,所以在100g水中加入100g甲,充分溶解后溶液的质量是160g,故B错误;
C、40℃时,甲、乙两种物质的溶解度相等,所以甲、乙两种物质饱和溶液中溶质的质量相等,故C正确;
D、乙物质的溶解度随温度的升高而减小,所以采用升温的方法可将乙的不饱和溶液转化为饱和溶液,故D正确.
故选:B.
点评 本题难度不是很大,主要考查了固体溶解度曲线的意义及根据固体的溶解度曲线解决相关的问题.

练习册系列答案
相关题目
15. 如图是A、B、C三种物质的溶解度曲线,下列分析错误的是( )
如图是A、B、C三种物质的溶解度曲线,下列分析错误的是( )
 如图是A、B、C三种物质的溶解度曲线,下列分析错误的是( )
如图是A、B、C三种物质的溶解度曲线,下列分析错误的是( )| A. | 50℃时,A物质的溶解度最大 | |
| B. | 50℃时,把90gA物质放入100g水中能得到190g溶液 | |
| C. | 20℃时,B物质饱和溶液的溶质质量分数最大 | |
| D. | 升温可使C物质的不饱和溶液变成饱和溶液 |
12.除去下列物质中的杂质所选用的试剂及操作方法正确的一组是( )
| 选项 | 物 质 | 所含杂质 | 除 去 杂 质 的 方 法 |
| A | Cu | CuO | 加入过量的稀硫酸、过滤、洗涤、干燥 |
| B | N2 | O2 | 放入足量的红磷后点燃 |
| C | NaCl溶液 | NaOH | 加入适量稀盐酸,蒸发、结晶 |
| D | FeSO4 | CuSO4 | 先加水溶解,再加足量金属铁,过滤,洗涤,干燥 |
| A. | A | B. | B | C. | C | D. | D |
19.3月22日是“世界水日“.下列有关水的叙述正确的是( )
| A. | 生活中通过煮沸可以降低水的硬度 | |
| B. | 经常饮用蒸馏水对身体有益无害 | |
| C. | 水中Ca2+、Mg2+增多导致水体富营养化 | |
| D. | 水是由氢气、氧气组成的 |
2.工业生产的纯碱中常常含有一定量的氯化钠.为了测定某批次纯碱中碳酸钠的质量分数,小明同学称取12g纯碱样品放入烧杯中,用相同溶质质量分数的稀盐酸50g,分5次加入,每次充分反应后,称重、计算生成二氧化碳的质量,记录如下:
请回答:
(1)在第四次实验中,碳酸钠完全反应.
(2)求所取样品中碳酸钠的质量分数(计算结果保留一位小数).
| 实验次数 | 稀盐酸用量(g) | 生成二氧化碳的质量(g) |
| 1 | 10 | 1.1 |
| 2 | 10 | 2.2 |
| 3 | 10 | 3.3 |
| 4 | 10 | 4.4 |
| 5 | 10 | 4.4 |
(1)在第四次实验中,碳酸钠完全反应.
(2)求所取样品中碳酸钠的质量分数(计算结果保留一位小数).
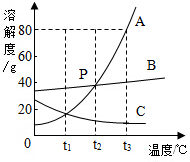 如图是A、B、C三种物质的溶解度曲线,回答下列问题:
如图是A、B、C三种物质的溶解度曲线,回答下列问题: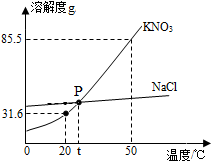 如图为NaCl和KNO3的溶解度曲线,请回答下列问题:
如图为NaCl和KNO3的溶解度曲线,请回答下列问题: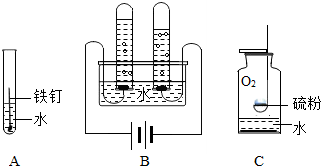 水是生命的源泉,下列变化都是与水相关,请根据A、B、C、D图示回答下列问题:
水是生命的源泉,下列变化都是与水相关,请根据A、B、C、D图示回答下列问题:
 ”所代表的物质与单质铁发生化合反应的化学方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,能观察到的现象是剧烈燃烧,火星四射,生成黑色固体.
”所代表的物质与单质铁发生化合反应的化学方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,能观察到的现象是剧烈燃烧,火星四射,生成黑色固体.