题目内容
课外小组对一批铁样品(含有杂质,杂质不溶于水,也不与稀硫酸反应)进行分析,甲、乙、丙三位同学分别进行实验,实验数据如下表:
| 甲 | 乙 | 丙 | |
| 烧杯+稀硫酸 | 150g | 100g | 100g |
| 加入的铁样品 | 6g | 6g | 10g |
| 充分反应后,烧杯+剩余物 | 155.8g | 105.8g | 109.8g |
(1)三位同学中________(填甲、乙或丙)所取的稀硫酸与铁样品恰好完全反应;
(2)计算样品中铁的质量分数;
(3)计算恰好完全反应后所得溶液中溶质的质量分数.(烧杯的质量为25.4g)
解:(1)由分析可知,所用样品最少的同学所取用的稀硫酸与铁样品恰好完全反应.故答案为:乙;
(2)(3)解:设样品中铁的质量为x,生成的FeSO4的质量为y,
Fe+H2SO4=FeSO4+H2↑
56 152 2
x y 0.2g
 =
= 解得 x=5.6 g 样品中铁的质量分数为:
解得 x=5.6 g 样品中铁的质量分数为: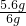 ×100%=93.3%;
×100%=93.3%;
 =
=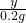 解得 y=15.2 g
解得 y=15.2 g
溶液中溶质质量分数=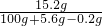 ×100%≈14.4%.
×100%≈14.4%.
答:样品中铁的质量分数为93.3%.生成的FeSO4溶液的质量分数为14.4%.
分析:(1)根据质量守恒定律、图表信息,三位同学的实验结果都生成了0.2g气体,推断所用样品最少的同学所取用的稀硫酸与铁样品恰好完全反应;
(2)(3)根据铁与硫酸反应的化学方程式和生成的其氢气的质量,列出比例式,就可计算出样品中铁的质量和生成的FeSO4的质量.然后根据质量分数公式计算即可.
点评:本题主要考查学生运用化学方程式和质量分数公式进行计算的能力,溶液和化学反应融合的题目,是综合性的题型,要求比较高.通常学生在计算时常常会忽视了实际参加反应的是溶液中溶质的质量,这就要求学生足够细心、会分析、且条理分明.
(2)(3)解:设样品中铁的质量为x,生成的FeSO4的质量为y,
Fe+H2SO4=FeSO4+H2↑
56 152 2
x y 0.2g
 =
= 解得 x=5.6 g 样品中铁的质量分数为:
解得 x=5.6 g 样品中铁的质量分数为: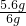 ×100%=93.3%;
×100%=93.3%; =
=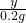 解得 y=15.2 g
解得 y=15.2 g溶液中溶质质量分数=
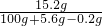 ×100%≈14.4%.
×100%≈14.4%.答:样品中铁的质量分数为93.3%.生成的FeSO4溶液的质量分数为14.4%.
分析:(1)根据质量守恒定律、图表信息,三位同学的实验结果都生成了0.2g气体,推断所用样品最少的同学所取用的稀硫酸与铁样品恰好完全反应;
(2)(3)根据铁与硫酸反应的化学方程式和生成的其氢气的质量,列出比例式,就可计算出样品中铁的质量和生成的FeSO4的质量.然后根据质量分数公式计算即可.
点评:本题主要考查学生运用化学方程式和质量分数公式进行计算的能力,溶液和化学反应融合的题目,是综合性的题型,要求比较高.通常学生在计算时常常会忽视了实际参加反应的是溶液中溶质的质量,这就要求学生足够细心、会分析、且条理分明.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
课外小组对一批铁样品(含有杂质,杂质不溶于水,也不与稀硫酸反应)进行分析,甲、乙、丙三位同学分别进行实验,实验数据如下表:
请认真分析数据,回答下列问题:
(1)三位同学中______(填甲、乙或丙)所取的稀硫酸与铁样品恰好完全反应;
(2)计算样品中铁的质量分数;
(3)计算恰好完全反应后所得溶液中溶质的质量分数.(烧杯的质量为25.4g)
| 甲 | 乙 | 丙 | |
| 烧杯+稀硫酸 | 150g | 100g | 100g |
| 加入的铁样品 | 6g | 6g | 10g |
| 充分反应后,烧杯+剩余物 | 155.8g | 105.8g | 109.8g |
(1)三位同学中______(填甲、乙或丙)所取的稀硫酸与铁样品恰好完全反应;
(2)计算样品中铁的质量分数;
(3)计算恰好完全反应后所得溶液中溶质的质量分数.(烧杯的质量为25.4g)