题目内容
11. 化学是研究物质的组成、结构、性质及变化规律的科学.
化学是研究物质的组成、结构、性质及变化规律的科学.(1)比较下列两种变化:①水加热变成水蒸气;②水通电生成氢气和氧气.从微观粒子的角度分析,两种变化的本质区别是是否生成新分子.
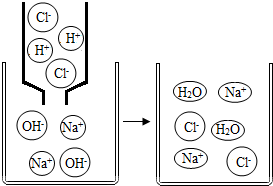
(2)如图是稀盐酸和氢氧化钠溶液发生化学反应的微观过程示意图,该反应的实质是H+和OH-反应生产水.
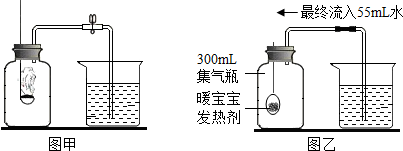
(3)为维护食品安全,禁止向面粉中添加过氧化钙(CaO2)作为增白剂.过氧化钙和水反应能生成一种碱和氧气,反应的化学方程式为2CaO2+2H2O=2Ca(OH)2+O2↑.
分析 (1)可以根据分子在物理变化和化学变化中的变化过程方面进行分析、判断,从而得出正确的结论;
(2)由盐酸与氢氧化钠溶液反应的微观过程示意图,从构成从微观粒子的角度分析该反应酸与碱中和的实质;
(3)根据反应原理写出反应的化学方程式解答.
解答 解:(1)水受热变成水蒸气,是水分子之间的间隔增大,水分子本身没有发生变化,属于物理变化;而水通电后被分解为氧原子和氢原子,每两个氧原子构成一个氧分子,每两个氢原子构成一个氢分子,大量的氧分子聚集成为氧气,大量的氢分子聚集成为氢气,该变化属于化学变化.
(2)由盐酸与氢氧化钠溶液反应的微观过程示意图可知,从微观粒子的角度分析,该反应酸与碱中和的实质为:氢离子和氢氧根离子结合生成水分子;
(3)过氧化钙和水反应能生成一种碱和氧气,反应的化学方程式为:2CaO2+2H2O=2Ca(OH)2+O2↑.
答案:
(1)是否生成新分子;
(2)H+和OH-反应生产水;
(3)2CaO2+2H2O=2Ca(OH)2+O2↑.
点评 本题难度较大,综合性较强,考查了粒子结构示意图、分子在物理变化和化学变化中的变化实质、中和反应的实质等,完成此题,可以依据已有的课本知识进行.

练习册系列答案
相关题目
2.化学与生活的密切关系.下列有关说法中正确的是( )
| A. | 碳酸钠俗名也叫苏打,可用于清洗厨房用具上的油污 | |
| B. | 青铜是我国使用最早的合金材料,目前世界上年产量最大的金属材料是铝 | |
| C. | 明矾[KAl(SO4)2•12H2O]溶于水会形成胶体,因此可用于自来水的消毒杀菌 | |
| D. | 利用石油中各成分沸点不同进行分馏生产出柴油属于化学变化 |
19.关于人体所需的营养物质,下列叙述错误的是( )
| A. | 蛋白质、糖类都属于有机物 | B. | 人体缺钙易引起甲状腺肿大 | ||
| C. | 糖类由C、H、O三种元素组成 | D. | 脂肪是维持生命活动的备用能源 |
6. 小明用如图装置进行实验,下列有关说法正确的是( )
小明用如图装置进行实验,下列有关说法正确的是( )
 小明用如图装置进行实验,下列有关说法正确的是( )
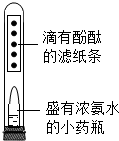
小明用如图装置进行实验,下列有关说法正确的是( )| A. | 该实验能证明分子在不断的运动 | |
| B. | 将装置浸入冰水中,滤纸条不变红 | |
| C. | 滤纸条上的酚酞由上到下依次变红 | |
| D. | 仅将浓氨水换成浓盐酸也可达到实验目的 |
16.某小组在学习“二氧化碳制取的研究”课题时,探究了二氧化碳气体的收集方法.
【提出问题】二氧化碳能不能用排水法收集?
【查阅资料】
①通常状况下,1 体积水约能溶解1 体积二氧化碳,所得溶液pH约为5.6.
②HCl气体极易溶于水.
【设计方案】
方案一:在通常状况下,通过测定二氧化碳溶于水所得溶液的pH,判断二氧化碳在水中溶解的体积,实验装置如下图所示,装置气密性良好.

(1)实验前,K1、K2、K3均关闭.实验时,需先将甲装置中的空气排尽,其操作是,打开活塞,滴加足量稀盐酸,关闭活塞.检验空气已排尽的方法是打开K1,将燃着的木条放在a口处,若木条熄灭则空气已经排尽.
(2)关闭K1,打开K2、K3.待丙装置中收集半瓶气体时,关闭K2和K3,充分振荡丙装置.然后用pH计测得如下数据:
分析可知,丙装置所溶解二氧化碳的体积大于(填“大于”、“小于”或“等于”)丁装置溶解二氧化碳的体积.
(3)实验中,若没有乙装置,则测出的溶液pH会偏小(填“偏大”或“偏小”).
方案二:在通常状况下,用氧气测量仪分别测定排空气法和排水法收集的二氧化碳气体中氧气的体积分数,测得的数据如下图所示.
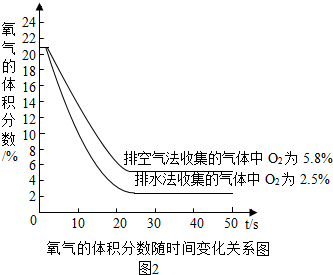
(4)两种方法收集的气体中二氧化碳体积分数较大的是排水(填“排空气”或“排水”)法.
【反思评价】
(5)方案二中两种方法收集的二氧化碳气体中的氧气来自于空气,两种方法收集的气体中二氧化碳体积分数的差值是15.7%.
【提出问题】二氧化碳能不能用排水法收集?
【查阅资料】
①通常状况下,1 体积水约能溶解1 体积二氧化碳,所得溶液pH约为5.6.
②HCl气体极易溶于水.
【设计方案】
方案一:在通常状况下,通过测定二氧化碳溶于水所得溶液的pH,判断二氧化碳在水中溶解的体积,实验装置如下图所示,装置气密性良好.

(1)实验前,K1、K2、K3均关闭.实验时,需先将甲装置中的空气排尽,其操作是,打开活塞,滴加足量稀盐酸,关闭活塞.检验空气已排尽的方法是打开K1,将燃着的木条放在a口处,若木条熄灭则空气已经排尽.
(2)关闭K1,打开K2、K3.待丙装置中收集半瓶气体时,关闭K2和K3,充分振荡丙装置.然后用pH计测得如下数据:
| 物质 | 丙装置中溶液 | 丁装置中溶液 |
| pH | 5.60 | 6.50 |
(3)实验中,若没有乙装置,则测出的溶液pH会偏小(填“偏大”或“偏小”).
方案二:在通常状况下,用氧气测量仪分别测定排空气法和排水法收集的二氧化碳气体中氧气的体积分数,测得的数据如下图所示.

(4)两种方法收集的气体中二氧化碳体积分数较大的是排水(填“排空气”或“排水”)法.
【反思评价】
(5)方案二中两种方法收集的二氧化碳气体中的氧气来自于空气,两种方法收集的气体中二氧化碳体积分数的差值是15.7%.
20.氢氧化钠和氢氧化钙是两种常见的碱.李红同学将两种碱的溶液分别装入试管A、B中,并进行了如图所示的三组实验.
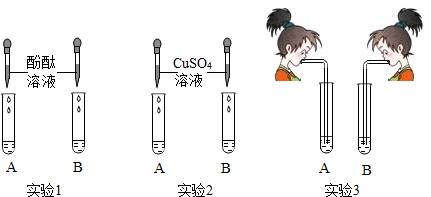
(1)实验l中,两支试管的溶液都变成红色.
(2)实验2中,若B盛装的是NaOH溶液,发生反应的化学方程式为2NaOH+CuSO4═Cu(OH)2↓+Na2SO4.
(3)实验3中,李红同学向两支试管吹气,A中有白色沉淀生成,发生反应的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O.
B中无现象,为了探究吹气后B中溶质的成分,李红进行了如下探究.
提出猜想:
猜想1:溶质只有氢氧化钠
猜想2:溶质只有碳酸钠
猜想3:溶质有氢氧化钠和碳酸钠
【实验和结论】:
反思与评价:
老师评价李红得出的结论不正确,是因为猜想2(填数字)也会产生相同的现象.如果要验证“猜想3成立”,必须要换试剂,将氢氧化钙溶液换成氯化钙溶液.

(1)实验l中,两支试管的溶液都变成红色.
(2)实验2中,若B盛装的是NaOH溶液,发生反应的化学方程式为2NaOH+CuSO4═Cu(OH)2↓+Na2SO4.
(3)实验3中,李红同学向两支试管吹气,A中有白色沉淀生成,发生反应的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O.
B中无现象,为了探究吹气后B中溶质的成分,李红进行了如下探究.
提出猜想:
猜想1:溶质只有氢氧化钠
猜想2:溶质只有碳酸钠
猜想3:溶质有氢氧化钠和碳酸钠
【实验和结论】:
| 实验 | 实验现象 | 结论 |
| 取B中少量溶液,加人澄清石灰水至不再 产生沉淀为止,过滤后取上层清液, 向其中加几滴酚酞试液. | 产生白色沉淀 溶液呈现红色 | 猜想3成立 |
老师评价李红得出的结论不正确,是因为猜想2(填数字)也会产生相同的现象.如果要验证“猜想3成立”,必须要换试剂,将氢氧化钙溶液换成氯化钙溶液.