题目内容
10.如图表示M、N两种固体物质的溶解度曲线,下列对图示信息的描述正确的是( )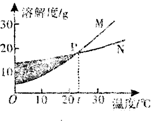
| A. | 30℃时M的溶解度小于N的溶解度 | |
| B. | 分离M、N可采用蒸发结晶的方法 | |
| C. | M、N都是难溶物质 | |
| D. | 阴影处各点对应的溶液(不包含曲线上的点)是N的不饱和溶液,M的饱和溶液 |
分析 根据题目信息和溶解度曲线可知:M、N种固体物质的溶解度,都是随温度升高而增大,而M的溶解度随温度的升高变化比N大;30℃时M的溶解度小于N的溶解度,小于不正确;分离M、N可采用降温结晶的方法,蒸发结晶不可行;M、N都是难溶物质错误,它们都是易溶物质;阴影处各点对应的溶液(不包含曲线上的点)是N的不饱和溶液,M的饱和溶液正确.
解答 解:A、30℃时M的溶解度小于N的溶解度,小于不正确;故选项错误;
B、分离M、N可采用降温结晶的方法,蒸发结晶不可行,故选项错误;
C、M、N都是难溶物质错误,它们都是易溶物质,故选项错误;
D、阴影处各点对应的溶液(不包含曲线上的点)是N的不饱和溶液,M的饱和溶液正确,故选项正确;
故选D
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液结晶的方法,本考点主要出现在选择题和填空题中.

练习册系列答案
相关题目
8.区别下列各组物质,选择的实验方法不能达到目的是( )
| A. | CO2和CO:闻气味 | |
| B. | 黄铜片和铜片:相互刻画 | |
| C. | 浓盐酸和浓硫酸:分别用玻璃棒蘸取点在滤纸上 | |
| D. | BaCl2溶液和KNO3溶液:分别加入Na2SO4溶液 |
9.把相同质量分数的稀盐酸分别滴加到A、B、C三种金属中,A表面有气泡产生,B、C始终无明显变化;把B的硝酸盐溶液滴加到C中,C表面析出B.则三种金属活动性质顺序为( )
| A. | A>C>B | B. | C>B>A | C. | B>C>A | D. | C>A>B |
5.碲(Te)被誉为“现代工业、国防与尖端技术的维生素,创造人间奇迹的桥梁”实验室模拟提取碲的一个实验是:取某含碲溶液于烧瓶中,加入适量NaC1,加热到一定温度,持续通入SO2,待反应一定时间,过滤得到粗碲.
(1)反应的总化学方程式为:TeOSO4+2SO2+3X$\frac{\underline{\;\;△\;\;}}{\;}$Te↓+3H2SO4,则X为H2O(填化学式).
(2)为探究获得较高粗碲沉淀率的反应条件,某研究小组在控制NaC1浓度和SO2流量不变的条件下,进行下述对比试验,数据如下:
①该小组研究的反应条件是温度和反应时间.
②实验a和b的目的是比较相同时间,不同的反应温度对粗碲沉淀率的影响.
③在上述四组实验中,最佳的反应条件是80℃和2.0h.
④为了提升设备利用效率和节约能源,可进一步优化反应条件测定粗碲沉淀率.若再设计对比实验,选择的反应条件还可以是A(填选项).
A.80℃,1.5h B.80℃,2.5h C.70℃,2.0h D.95℃,2.0h.
(1)反应的总化学方程式为:TeOSO4+2SO2+3X$\frac{\underline{\;\;△\;\;}}{\;}$Te↓+3H2SO4,则X为H2O(填化学式).
(2)为探究获得较高粗碲沉淀率的反应条件,某研究小组在控制NaC1浓度和SO2流量不变的条件下,进行下述对比试验,数据如下:
| 实验 | 温度/ | 反应时间/h | 粗蹄沉淀率 |
| A | 65 | 3.0 | 65.0 |
| B | 80 | 3.0 | 98.9 |
| C | 80 | 2.0 | 98.9 |
| d | 90 | 2.0 | 97.0 |
②实验a和b的目的是比较相同时间,不同的反应温度对粗碲沉淀率的影响.
③在上述四组实验中,最佳的反应条件是80℃和2.0h.
④为了提升设备利用效率和节约能源,可进一步优化反应条件测定粗碲沉淀率.若再设计对比实验,选择的反应条件还可以是A(填选项).
A.80℃,1.5h B.80℃,2.5h C.70℃,2.0h D.95℃,2.0h.
15.将下列两种溶液混合,再加入足量的酸,最终有沉淀生成是( )
| A. | 碳酸钾和碳酸钙再加稀硝酸 | B. | 氯化铜和氢氧化钡再加盐酸 | ||
| C. | 硝酸银和氯化钠再加稀硝酸 | D. | 硝酸钠和硝酸银再加硫酸 |