题目内容
17.某同学在实验结束进行废液处理时,将碳酸钠溶液、稀盐酸倒入指定的洁净容器中,看到有气泡产生,待不再产生气泡时,又倒入了氢氧化钙溶液,发现该容器中有白色沉淀产生,这一现象引起了他的注意,为了解释以上三种物质之间的反应情况,他决定从反应后溶液中的溶质组成人手进行探究.(1)他对反应后溶液中的溶质组成作出了两种猜想:
猜想①:溶质为氯化钠、氢氧化钠;
猜想②:溶质为氯化钠、氢氧化钠、氢氧化钙;
请你再补充一种.猜想③:溶质为氯化钠、氢氧化钠、碳酸钠.
(2)比较三种猜想,说明该同学作出猜想①的理由碳酸钠与稀盐酸反应生成氯化钠;过量碳酸钠与氢氧化钙溶液恰好完全反应
(3)比较三种猜想的异同,如果猜想③成立,设计实验,用两种方法加以证明.按相关要求填写下表.
| 实验操作 | 实验现象 | |
| 方法一 | ||
| 方法二 |
分析 (1)①因为“碳酸钠溶液、稀盐酸倒入到指定的洁净容器中,看到有气泡产生”,所以反应生成氯化钠;②“又倒入了氢氧化钙溶液,发现该容器中有白色沉淀产生”,说明溶液中存在碳酸根,生成碳酸钙和氢氧化钠.③因为氢氧化钠溶液容易吸收空气中的二氧化碳,生成碳酸钠,所以猜想③:溶质为氯化钠、氢氧化钠、碳酸钠;
(2)因为碳酸钠溶液与盐酸反应,生成氯化钠、二氧化碳和水,待不再有气泡产生时,加入氢氧化钙溶液后,出现了白色沉淀,说明稀盐酸不足,碳酸钠有剩余;剩余的碳酸钠溶液与加入的氢氧化钙溶液恰好完全反应,生成氢氧化钠和碳酸钙沉淀.所以此时溶液中含有的溶质是氯化钠和氢氧化钠;
(3)如果猜想③成立,用两种方法设计实验,加以证明碳酸根进行检验.
解答 解:(1)由题意,做出三种不同的猜想,了解碳酸钠是否完全反应;碳酸钠溶液与盐酸反应,生成氯化钠、二氧化碳和水,待不再有气泡产生时,加入氢氧化钙溶液后,出现了白色沉淀,说明稀盐酸不足,碳酸钠有剩余,故猜想③:溶质为氯化钠、氢氧化钠、碳酸钠;故填:氯化钠、氢氧化钠、碳酸钠;
(2)碳酸钠溶液与盐酸反应,生成氯化钠、二氧化碳和水,待不再有气泡产生时,加入氢氧化钙溶液后,出现了白色沉淀,说明稀盐酸不足,碳酸钠有剩余;剩余的碳酸钠溶液与加入的氢氧化钙溶液恰好完全反应,生成氢氧化钠和碳酸钙沉淀.此时溶液中含有的溶质是氯化钠和氢氧化钠;故填:碳酸钠与稀盐酸反应生成氯化钠;过量碳酸钠与氢氧化钙溶液恰好完全反应;
(3)证明碳酸根离子的存在,可用稀盐酸或澄清的石灰水来检验;故填:
| 实验操作 | 实验现象 | |
| 方法一 | 滴加足量的稀盐酸 | 有气泡产生 |
| 方法二 | 滴加少量的石灰水 | 白色沉淀生成 |
点评 本题主要考查化学实验方案的设计与评价,学会运用猜想与事实验证的方法和技巧处理实验问题,掌握盐的化学性质.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
5.下列物质的用途由化学性质决定的是( )
| A. | 金刚石刻画玻璃 | B. | 木炭用作燃料 | ||
| C. | 石墨作干电池的电极 | D. | 活性炭除去冰箱内异味 |
9.下列各组中的三种物质,颜色彼此相同的一组是( )
| A. | 氢气、氮气、液态氧 | B. | 硫粉、铁丝、镁带 | ||
| C. | 二氧化锰、木炭、高锰酸钾 | D. | 氧化镁、碳酸氢铵、五氧化二磷 |
6.关于物质的转化过程:H2→H2O,CO→CO2,Cu→CuO.下列说法不正确的是( )
| A. | 都能通过化合反应实现 | |
| B. | 都能通过置换反应实现 | |
| C. | 都能通过与单质反应实现 | |
| D. | 变化前后某些元素的化合价发生改变 |
7.1g下列各种原子中,所含原子数目最少的是( )
| A. | 铁原子 | B. | 钠原子 | C. | 碳原子 | D. | 氢原子 |
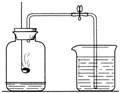 小军根据燃烧红磷测定空气中氧气含量的实验原理,用红磷测定空气中氧气的含量,并按如图所示装置进行实验.
小军根据燃烧红磷测定空气中氧气含量的实验原理,用红磷测定空气中氧气的含量,并按如图所示装置进行实验. 