题目内容
14.硅钢可用于制造变压器的铁芯,某化学兴趣小组的同学为了验证硅钢(主要含有Fe、C、Si),设计了如图的试验流程(有些反应的部分反应物和生成物已省略).查阅资料发现常温下,单质硅(Si)不能与盐酸反应,但能与氢氧化钠溶液反应(Si+2NaOH+H2O═Na2SiO2+2H2↑).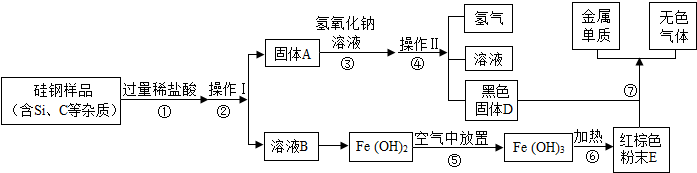
根据以上信息,回答下列问题:
(1)操作Ⅰ、Ⅱ的名称为过滤,硅钢样品反应前须粉碎目的是增大反应物的接触面积;
(2)滤液B中的溶质为FeCl2、HCl;
(3)写出步骤⑦中发生反应的化学方程式3C+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑;其基本反应类型为置换反应;
(4)步骤⑤中发生的是化合反应,尝试写出其化学方程式4Fe(OH)2+O2+2H2O=4Fe(OH)3.
分析 (1)根据过滤的操作分析;
(2)根据硅钢成分以及与盐酸反应情况解答;
(3)碳还原氧化铁生成铁和二氧化碳写化学方程式,判断反应类型;
(4)根据Fe(OH)2在空气中与氧气和水反应写化学方程式.
解答 解:(1)操作Ⅰ、Ⅱ是将固体和液体的分离,因此是过滤;硅钢样品反应前须粉碎可以增大反应物的接触面积;
(2)硅钢中主要含有Fe、C、Si,只有Fe能与稀盐酸反应生成氯化亚铁,故剩余的固体A的成分中含有C、Si,滤液B中含有氯化亚铁及过量的盐酸;
(3)根据碳还原氧化铁生成铁和二氧化碳,故反应的化学方程式为3C+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑;该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应;
(4)反应物是Fe(OH)2与氧气和水,写在等号的左边,生成物是氢氧化铁写在等号的右边,用观察法配平即可,所以反应的化学方程式是:4Fe(OH)2+O2+2H2O=4Fe(OH)3.
故答案为:(1)过滤;增大反应物的接触面积;
(2)FeCl2、HCl;
(3)3C+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑;置换反应;
(4)4Fe(OH)2+O2+2H2O=4Fe(OH)3
点评 解答本题关键是要知道回收金属时,是利用排在盐中金属元素前面的金属把盐中的金属元素置换出来,为了反应完全,要加入过量的金属,固体中会混有置换出来的金属和过量的金属,再利用二者性质的不同进行分离.

练习册系列答案
相关题目
4.下列有关原子的说法中错误的是( )
| A. | 原子之间也存在间隔 | B. | 原子总是不断运动着的 | ||
| C. | 原子可以构成分子 | D. | 原子很小,不可以再分 |
2.甲、乙两种固体物质的溶解度曲线如图所示,下列有关叙述中错误的是( )
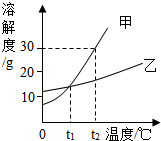

| A. | t1℃时,甲、乙物质的溶解度相等 | |
| B. | t2℃时,甲饱和溶液的溶质的质量分数为30% | |
| C. | 升高温度可以使乙的饱和溶液变为不饱和溶液 | |
| D. | 甲中混有少量的乙,可采用冷却热饱和溶液的方法分离 |
19.在pH=1的溶液中能大量共存,并且溶液为无色透明的离子组是( )
| A. | Ba2+、Na+、NO3-、SO${\;}_{4}^{2-}$ | B. | K+、Cl-、CO32-、NO3- | ||
| C. | Mg2+、Cl-、Al3+、NO3- | D. | Ca2+、Na+、Fe3+、NO3- |
3.如图是钠的原子结构示意图.下列说法不正确的是( )
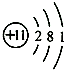

| A. | 钠属于金属元素 | B. | 钠原子的质子数为11 | ||
| C. | 钠离子的符号为Na+ | D. | 钠在化学反应中易得到电子 |
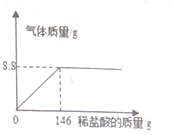 化学研究小组为测定某石灰石样品中碳酸钙的质量分数,取25g石灰石样品放在烧杯中,然后向其中逐滴加入一定量某质量分数的稀盐酸,使之与样品充分反应(杂质不参加反应).随着反应进行,加入稀盐酸的质量与反应得到气体的质量变化关系如图所示.请完成下列计算内容:
化学研究小组为测定某石灰石样品中碳酸钙的质量分数,取25g石灰石样品放在烧杯中,然后向其中逐滴加入一定量某质量分数的稀盐酸,使之与样品充分反应(杂质不参加反应).随着反应进行,加入稀盐酸的质量与反应得到气体的质量变化关系如图所示.请完成下列计算内容: