题目内容
3.金属铁密度小、硬度大、抗腐蚀性能好,被誉为“未来的金属”,某工厂用钛酸亚铁(FeTiO3)、焦炭为原料制取金属钛,请据图回答下列问题: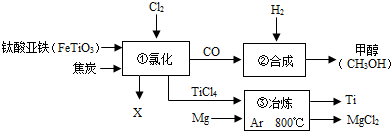
(1)反应前将钛酸亚铁和焦炭磨成粉末状的原因是为了增大反应物之间的接触面积,钛酸亚铁(FeTiO3)中钛元素为+4价.
(2)Ti2O2与C、Cl2在高温下反应,生成TiCl4和一种有毒气体,该气体是一种氧化物,其化学式为CO.
(3)写出步骤③中(Ar起保护气作用)在高温时生成金属钛的化学反应方程式TiCl4+2Mg$\frac{\underline{\;高温\;}}{\;}$Ti+2MgCl2,该反应的基本类型为置换反应.
(4)今年来,工业上用电解熔融的TiO2来制取金属Ti获得成功,从能量的角度分析,工业利用该方法制备金属Ti的缺点是需要消耗大量的电能.
分析 (1)根据反应物之间的接触面积以及化合价的计算方法来分析;
(2)根据化学反应前后原子的种类和数目不变求物质的化学式;
(3)根据题中信息结合化学方程式的书写分析;
(4)根据反应的条件来分析.
解答 解:(1)反应前将钛酸亚铁和焦炭磨成粉末状是为了增大反应物之间的接触面积;钛酸亚铁的化学式为FeTiO3,其中铁元素的化合价为+2价,氧元素的化合价为-2价,因化合物中元素化合价的代数和为0,设钛的化合价为x,则(+2)+x+(-2)×3=0,解得x=+4.故答案为:为了增大反应物之间的接触面积;+4;
(2)Ti2O2与C、Cl2在高温下反应,生成TiCl4和一种有毒气体,该气体是一种氧化物,该气体是一氧化碳,故填:CO;
(3)根据题中信息,镁与TiCl4在高温条件下反应生成金属钛和氯化镁,该反应的化学方程式为TiCl4+2Mg$\frac{\underline{\;高温\;}}{\;}$Ti+2MgCl2;该反应是由一种单质与一种化合物反应生成另一种单质与另一种化合物,属于置换反应;故答案为:TiCl4+2Mg$\frac{\underline{\;高温\;}}{\;}$Ti+2MgCl2;置换反应;
(4)工业上用电解熔融的TiO2来制取金属Ti获得成功,但是此方法需要消耗大量的电能,故填:需要消耗大量的电能.
点评 本题考查物质的制备实验方案的设计,侧重于学生的分析能力和实验能力的考查,为高考常见题型,难度中等,注意把握实验的基本原理和物质的性质.

练习册系列答案
相关题目
13.如表是KCl和KNO3在不同温度下的溶解度.
①硝酸钾的溶解度随温度的升高而增大(填“增大”或“减小”).
②用同一种方法可以使KCl、KNO3二种物质的溶液都析出晶体,该方法是蒸发结晶.
③KCl、KNO3两种物质溶解度相等的温度在B之间(用编号表示)
A.20℃以下B.20℃~30℃C.30℃~40℃D.40℃~50℃
④20℃时,100g水中最多可溶解KCl34.0g;40℃时,将70g KCl的饱和溶液稀释成质量分数为20%的溶液,需加水30g.
⑤将某温度下热的硝酸钾饱和溶液逐渐冷却至室温,下列有关量随时间变化趋势的图象不正确的是D(用编号表示)

⑥实验设计:将不饱和氯化钾溶液变为饱和溶液
| 温度/℃ | 20 | 30 | 40 | 50 | |
| 溶解度(g/100g水) | KCl | 34.0 | 37.0 | 40.0 | 42.6 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | |
②用同一种方法可以使KCl、KNO3二种物质的溶液都析出晶体,该方法是蒸发结晶.
③KCl、KNO3两种物质溶解度相等的温度在B之间(用编号表示)
A.20℃以下B.20℃~30℃C.30℃~40℃D.40℃~50℃
④20℃时,100g水中最多可溶解KCl34.0g;40℃时,将70g KCl的饱和溶液稀释成质量分数为20%的溶液,需加水30g.
⑤将某温度下热的硝酸钾饱和溶液逐渐冷却至室温,下列有关量随时间变化趋势的图象不正确的是D(用编号表示)

⑥实验设计:将不饱和氯化钾溶液变为饱和溶液
| 实验步骤 | 实验现象 | 实验结论 |
| 向不饱和的氯化钾溶液 中不断加入氯化钾固体 | 有固体不再溶解 | KCl不饱和溶液 变为饱和溶液 |
18. 铬是重要的合金元素,镀在金属上可以防锈,元素周期表中“铬”的信息如图所示,下列关于铬元素说法正确的是( )
铬是重要的合金元素,镀在金属上可以防锈,元素周期表中“铬”的信息如图所示,下列关于铬元素说法正确的是( )
 铬是重要的合金元素,镀在金属上可以防锈,元素周期表中“铬”的信息如图所示,下列关于铬元素说法正确的是( )
铬是重要的合金元素,镀在金属上可以防锈,元素周期表中“铬”的信息如图所示,下列关于铬元素说法正确的是( )| A. | 是非金属元素 | B. | 原子序数为24 | ||
| C. | 相对原子质量为52.00g | D. | 中子数为24 |
 NaCl、KN03两种物质的溶液度曲线图如图所示,请回答:
NaCl、KN03两种物质的溶液度曲线图如图所示,请回答:
 用木炭还原氧化铜的实验,如图所示:
用木炭还原氧化铜的实验,如图所示: