题目内容
实验室常用加热氯酸钾和二氧化锰混合物的方法制取氧气,写出反应的文字或符号表达式: 。
小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂。
【完成实验】按下表进行分析:测定分解温度(分解温度越低,催化效果越好)。
实验编号 | 实验药品 | 分解温度(℃) |
① | 氯酸钾 | 580 |
② | 氯酸钾、二氧化锰(质量比1:1) | 未测 |
③ | 氯酸钾、氧化铜(质量比l:1) | 370 |
④ | 氯酸钾、氧化铁(质量比1:1) | 390 |
【分析数据、得出结论】
(1)由实验_____________与实验④对比,证明猜想合理。
(2)已知实验所用的三种物质中,催化效果最好的是二氧化锰,则实验②的分解温度 370(填“>”、“=”或“<”)。
【反思】
(1)若要证明氧化铁是该反应的催化剂,还要验证它在化学反应前后质量和 不变;
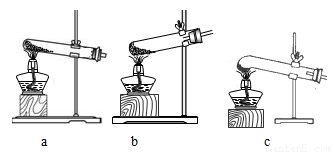
(2)已知氯酸钾的熔点为356℃,结合上表数据,你认为加热氯酸钾和氧化铁的混合物制氧气最适宜的装置是 (填字母)
(3)同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证
 名校课堂系列答案
名校课堂系列答案某同学发现一瓶没有塞上瓶塞的过氧化氢溶液。查资料得知,过氧化氢溶液在光线的直射下也能分解成氧气和水。他想探究这瓶过氧化氢溶液是否已经完全分解,与同学们一起进行如下实验。
【猜想与假设】
猜想Ⅰ:这瓶过氧化氢溶液已经完全分解。 猜想Ⅱ:这瓶过氧化氢溶液未完全分解。
【设计实验】为了验证猜想,甲、乙、丙三位同学分别提出如下方案:
甲同学:取适量试剂于试管中,伸入带火星的木条,若带火星的木条复燃,则猜想Ⅰ成立,若带火星的木条不复燃,则猜想Ⅱ成立。同学们认为此方案不行,原因是_______________________。
乙同学:取等量的过氧化氢溶液于A、B两个试管中,向A试管中加入少量二氧化锰,再把带火星的木条分别伸入A、B试管中,若观察到_____________________,则猜想Ⅰ成立。该实验中,B试管的作用是_____________。
丙同学:
操作 | 现象 | 结论 |
取与甲同学等量的试剂于另一支试管中,加热,再伸入带火星的木条 | _______________________ , ________________________ | 猜想Ⅱ 成立 |
【反思与交流】
① 敞口放置的试剂容易变质,所以要_________保存;过氧化氢溶液见光易分解,所以要存放在___________(填试剂瓶类型)中。
② 二氧化锰在过氧化氢的分解中起催化作用。从本组实验中可得知,能改变化学反应速率的方法还可以_______________________。