题目内容
7.下面二个实验采用对比的实验方法进行探究.(1)用实验一图1所示装置进行二氧化性质的探究.
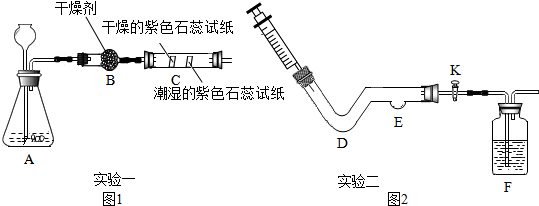
当长颈漏斗中的稀盐酸与锥形瓶中的大理石接触后,有大量气泡产生,该反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑;C中观察到的现象是干燥的石蕊试纸不变色,潮湿的石蕊试纸变红.
(2)用实验二图2所示装置进行燃烧条件的探究.
在D处放二氧化锰,E处放木炭,F中装澄清石灰水.为验证可燃物燃烧的两个条件,进行如下实验:
①打开K,用注射器注入一定量氮气,在E处点燃酒精灯加热木炭,木炭不燃烧,此操作目的是证明燃烧需要氧气.
②一段时间后,用注射器注入足量的过氧化氢溶液,同时打开K,D处产生气体,D处反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.木炭不燃烧,澄清石灰水未变浑浊.在E处点燃酒精灯,观察到木炭燃烧,澄清石灰水变浑浊,F处发生反应的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O.此操作目的是证明可燃物的温度要达到着火点才会燃烧.
分析 根据碳酸钙与盐酸的反应以及二氧化碳的化学性质进行分析解答;根据燃烧的条件以及氧气的制取进行分析解答,二氧化碳能使澄清的石灰水变浑浊,据此解答.
解答 解:(1)大理石的主要成分是碳酸钙,与稀盐酸反应生成氯化钙、水和二氧化碳,方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;二氧化碳能与水反应生成碳酸,碳酸能使紫色的石蕊试液变红色,二氧化碳不能是干燥的试纸变色,故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;干燥的石蕊试纸不变色,潮湿的石蕊试纸变红;
(2)加热的木碳在充有氮气的环境中不能燃烧,说明物质燃烧需要氧气;过氧化氢在二氧化锰的作用下分解生成了氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;木炭燃烧,发白光,澄清石灰水变浑浊,说明木炭燃烧有二氧化碳产生,故C处发生反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O.有题目中的信息可知,未点燃木炭,木炭不燃烧,点燃木炭时,木炭燃烧,故此操作目的是验证燃烧需要温度达到自身的着火点.
故答案为:①证明燃烧需要氧气;
②2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;Ca(OH)2+CO2═CaCO3↓+H2O;证明可燃物的温度要达到着火点才会燃烧.
点评 本题主要考查了二氧化碳的性质和燃烧条件的探究,有一定的难度.掌握化学方程式的书写以及物质的性质、燃烧的条件是解答本题的关键.

练习册系列答案
相关题目
17.某研究小组对用H2O2分解生成H2O和O2的实验条件进行探究.他们进行了以下实验:
①往盛有5mL 5% H2O2溶液的试管中,伸入带火星的木条,木条不复燃.
②往盛有5mL w% H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条,木条复燃.
③往盛有5mL w% H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃.
④经检验,②、③中反应后试管中仍分别含有a g MnO2和a g Fe2O3.
问题:(1)MnO2、Fe2O3在上述反应中的作用是催化作用.
(2)实验 ②、④中H2O2的浓度(w%)以5%为宜.
研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究.下表选取了部分实验数据:
用足量等体积H2O2溶液制取相同体积O2所需的时间
(3)从上表中能得出哪些结论?
①往盛有5mL 5% H2O2溶液的试管中,伸入带火星的木条,木条不复燃.
②往盛有5mL w% H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条,木条复燃.
③往盛有5mL w% H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃.
④经检验,②、③中反应后试管中仍分别含有a g MnO2和a g Fe2O3.
问题:(1)MnO2、Fe2O3在上述反应中的作用是催化作用.
(2)实验 ②、④中H2O2的浓度(w%)以5%为宜.
研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究.下表选取了部分实验数据:
用足量等体积H2O2溶液制取相同体积O2所需的时间
 | 30% H2O2 | 15% H2O2 | 5% H2O2 |
| 加入a g MnO2 | 0.2 | 0.8 | 2.0 |
| 加入a g Fe2O3 | 7.0 | 9.0 | 16.0 |
12.某物质在空气中完全燃烧生成4.4g二氧化碳和2.7g水,则关于这种物质的组成描述正确的是( )
| A. | 该物质只含有碳元素和氢元素 | |
| B. | 该物质一定含有碳元素和氢元素可能含有氧元素 | |
| C. | 该物质中一定含有氧元素 | |
| D. | 该物质的分子中碳、氢原子的个数比为1:2 |
16.下列对实验结果的分析中,错误的是( )
| A. | 配制食盐溶液时,如果量取水时俯视读数,则所得溶液的溶质质量分数偏大 | |
| B. | 加热物质时,试管爆裂可能是试管外壁有水珠 | |
| C. | 将带燃着的木条伸入集气瓶内,木条熄灭,证明瓶内已集满二氧化碳 | |
| D. | 在测定空气中氧气的体积分数时,充分反应后,需将装置冷却至室温再读数,否则测量结果偏低 |
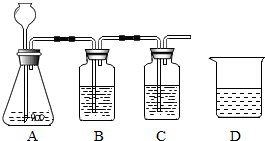 根据下列实验装置图回答问题:
根据下列实验装置图回答问题: