题目内容
5.下列各组物质的溶液相互间能发生中和反应且生成沉淀的是( )| A. | 氢氧化钠溶液和稀盐酸 | B. | 碳酸钠溶液和稀硫酸 | ||
| C. | 氢氧化钡溶液和稀硫酸 | D. | 氢氧化钠溶液和硝酸钾溶液 |
分析 分析题目有两个条件:一是两溶液混合后要发生中和,这需要从复分解反应的条件去判断;二是反应后生成沉淀.
解答 解:A、氢氧化钠溶液和稀盐酸反应生成氯化钠和水,没有沉淀,故错误;
B、碳酸钠溶液和稀硫酸反应生成硫酸钠、水和二氧化碳,该反应为盐与酸的反应,中和反应是酸与碱的反应,故该反应不属于中和反应;故错误;
C、氢氧化钡溶液和稀硫酸发生中和反应,且生成硫酸钡沉淀,故正确;
D、氢氧化钠溶液和硝酸钾溶液不反应,故错误.
故选:C.
点评 本题考查了中和反应的实质,可以从中和反应的定义进行分析,利用复分解反应的条件来判断反应能否发生.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.下列说法正确的是( )
| A. | 等质量的C和O2充分反应,生成物只有CO2 | |
| B. | 等质量的CO和CO2中,氧元素的质量比为11:14 | |
| C. | 等质量的H2O和H2O2分别制取氧气,H2O2生成的氧气质量大 | |
| D. | 等质量的Al和Mg分别与足量稀硫酸充分反应,生成H2的质量相等 |
10.溶液是生活中的常见现象,不同物质在水中的溶解能力不同.如表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g水).
(1)如表中的两种物质在40℃时,KNO3的溶解度较大;请用相应的数据列式表示该温度时KNO3饱和溶液的质量分数$\frac{63.9g}{63.9g+100g}×$100%(不要求计算).
(2)请写出一种将KNO3的不饱和溶液转化为饱和溶液的方法加入硝酸钾等(合理即可).
(3)20℃时,将20g NaCl放入50g水中,所得溶液的质量是68g.
(4)从NaCl溶液中得到NaCl晶体的方法是蒸发结晶.
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| NaCI | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
(2)请写出一种将KNO3的不饱和溶液转化为饱和溶液的方法加入硝酸钾等(合理即可).
(3)20℃时,将20g NaCl放入50g水中,所得溶液的质量是68g.
(4)从NaCl溶液中得到NaCl晶体的方法是蒸发结晶.
6.每年的4月22日是“世界地球日”.下列说法中与“世界地球日”的主题无关的是( )
| A. | 使用清洁能源作为燃料 | B. | 多植草种树 | ||
| C. | 分类回收垃圾,集中露天焚烧 | D. | 少开私家车,多坐公交车上班 |

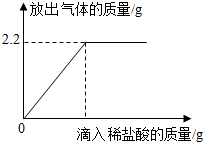 某混合物中含有碳酸钙和氯化钙,取该混合物8g,向其中滴加足量的稀盐酸,滴入稀盐酸的质量与放出气体质量之间的关系如图所示.计算所取混合物中碳酸钙的质量分数.
某混合物中含有碳酸钙和氯化钙,取该混合物8g,向其中滴加足量的稀盐酸,滴入稀盐酸的质量与放出气体质量之间的关系如图所示.计算所取混合物中碳酸钙的质量分数.