题目内容
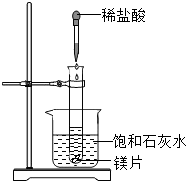 如图所示,把试管放在盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.请回答:
如图所示,把试管放在盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.请回答:(1)实验中能观察到哪些现象?
(2)产生上述现象的原因是什么?
(3)写出有关反应的化学方程式.
分析:运用镁和稀盐酸反应生成氢气同时放出大量的热,氢氧化钙溶解度随温度升高而减小解答.
解答:解:(1)镁和稀盐酸反应生成氢气同时放出大量的热,氢氧化钙溶解度随温度升高而减小,故(1)答案:向镁片表面产生气泡,逐渐减少;烧杯中有固体物质析出.
(2)镁和稀盐酸反应生成氢气同时放出大量的热,温度升高,氢氧化钙溶解度随温度升高而减小,故(2)答案镁跟盐酸反应产生氢气,并放出热量;Ca(OH)2的溶解度随温度的升高而变小.
(3)镁和稀盐酸反应生成氢气和氯化镁,故(3)答案:Mg+2HCl═MgCl2+H2↑
(2)镁和稀盐酸反应生成氢气同时放出大量的热,温度升高,氢氧化钙溶解度随温度升高而减小,故(2)答案镁跟盐酸反应产生氢气,并放出热量;Ca(OH)2的溶解度随温度的升高而变小.
(3)镁和稀盐酸反应生成氢气和氯化镁,故(3)答案:Mg+2HCl═MgCl2+H2↑
点评:同学们要会利用金属活动顺序表设计实验,去验证金属的还原性强弱.氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来,还要注意金属和酸反应产生氢气并放出热量.

练习册系列答案
 目标测试系列答案
目标测试系列答案
相关题目
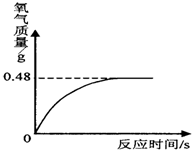 (1)雨桐同学用食品干燥剂制成的澄清石灰水,向其中吹入二氧化碳发现先产生沉淀,过一段时间后,发现沉淀溶解变成澄清溶液.为了确定沉淀溶解成澄清溶液的原因,同组的同学进行了相关探究.
(1)雨桐同学用食品干燥剂制成的澄清石灰水,向其中吹入二氧化碳发现先产生沉淀,过一段时间后,发现沉淀溶解变成澄清溶液.为了确定沉淀溶解成澄清溶液的原因,同组的同学进行了相关探究.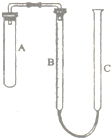 现有实验药品:一定质量的锌(片状或粒状)、浓硫酸(密度1.84g/cm3)、水以及如图所示装置.图中量气管是由B、C两根玻璃管组成,它们用橡皮管连通,并装适量水,B管有刻度(0-100mL),B、C管可固定在铁架上,供量气用;C管可上下移动,以调节液面高低.利用此装置可测定锌的相对原子质量.(设锌全部反应,产生的气体不超过50mL).
现有实验药品:一定质量的锌(片状或粒状)、浓硫酸(密度1.84g/cm3)、水以及如图所示装置.图中量气管是由B、C两根玻璃管组成,它们用橡皮管连通,并装适量水,B管有刻度(0-100mL),B、C管可固定在铁架上,供量气用;C管可上下移动,以调节液面高低.利用此装置可测定锌的相对原子质量.(设锌全部反应,产生的气体不超过50mL).