题目内容
某兴趣小组的同学为了测定碳酸钠样品(只含有氯化钠,不含其它杂质)中碳酸钠的含量,取该混合物样品与适量稀盐酸恰好完全反应,有关实验数据见附表.
附表:实验数据
| 反应前 | 反应后 | |||
| 实验数据 | 烧杯的质量/g | 稀盐酸的质量/g | 混合物样品的质量/g | 烧杯和其中混合物的质量/g |
| 40.6 | 123.4 | 12 | 171.6 |
(1)反应生成二氧化碳的质量为 g;
(2)样品碳酸钠的质量分数是多少?(最后结果保留到0.1%)
(3)反应后所得溶液的溶质质量分数是多少?
| 根据化学反应方程式的计算;有关溶质质量分数的简单计算. | |
| 专题: | 综合计算(图像型、表格型、情景型计算题). |
| 分析: | (1)根据化学方程式Na2CO3+2HCl═2NaCl+H2O+CO2↑,可知反应前后减少的质量就是生成二氧化碳的质量; (2)根据化学方程式和生成二氧化碳的质量可以计算出样品中Na2CO3的质量,进而求出该纯碱样品中Na2CO3的质量分数. |
| 解答: | 解:(1)根据化学方程式Na2CO3+2HCl═2NaCl+H2O+CO2↑,由质量守恒定律可知反应前后减少的质量就是生成二氧化碳的质量,是40.6g+123.4g+12g﹣171.6g=4.4g; (2)设样品中碳酸钠的质量为x,生成氯化钠的质量为y, Na2CO3+2HCl═2NaCl+H2O+CO2↑ 106 117 44 x y 4.4g x=10.6g; y=11.7g; 样品碳酸钠的质量分数是:=88%; (3)反应后所得溶液的溶质质量分数是:=10%; 答:(1)反应生成二氧化碳的质量为4.4g; (2)样品碳酸钠的质量分数是88%; (3)反应后所得溶液的溶质质量分数是10%; |
| 点评: | 要想解答好这类题目,要理解和熟记根据化学反应方程式的计算步骤、格式以及与之相关的知识等. |

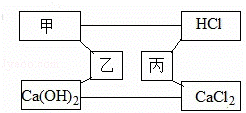
图中甲、乙、丙是初中化学常见的物质,用“﹣”连接的两种物质在溶液中可发生化学反应,下列说法不正确的是( )
|
| A. | 甲可以为盐 | B. | 乙只能是氧化物或酸 |
|
| C. | 丙只能是金属单质、盐或碱 | D. | 其中一个反应能同时生成两种沉淀 |
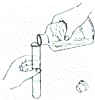
下列实验操作中正确的是( )
|
| A. |
取用金属颗粒 | B. |
倾倒液体 | C. |
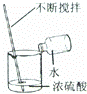
稀释浓硫酸 | D. |
二氧化碳验满 |

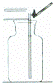
 e(OH)3
e(OH)3  的化学方程式是
的化学方程式是 A.2H2O2 MnO2 2H2O+O2↑
A.2H2O2 MnO2 2H2O+O2↑