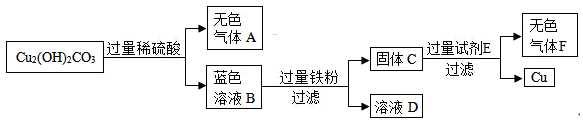
题目内容
3.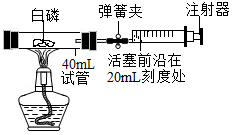 如图所示为测定空气中氧气含量的装置及药品:选用实际容积为40mL的直玻璃管作反应容器,将过量的白磷放入直玻璃管,用橡皮塞塞紧直玻璃管,再与容积为60mL且润滑性良好的针筒注射器组成实验装置.假设此装置能按照设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题:
如图所示为测定空气中氧气含量的装置及药品:选用实际容积为40mL的直玻璃管作反应容器,将过量的白磷放入直玻璃管,用橡皮塞塞紧直玻璃管,再与容积为60mL且润滑性良好的针筒注射器组成实验装置.假设此装置能按照设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题:(1)实验前,打开弹簧夹,将活塞前沿从注射器的20mL处推至15mL刻度处,然后松开手,若活塞依旧能回到20mL刻度处,则说明装置气密性好;
(2)若先夹紧弹簧夹,用酒精灯加热白磷,燃烧结束,等冷却到室温后打开弹簧夹.实验过程中可观察到的现象是注射器的活塞停在12mL;
(3)若不使用弹簧夹,用酒精灯加热白磷,充分反应直至燃烧结束,玻璃管冷却到室温.实验过程中可观察到的现象是注射器的活塞先向右移动,然后停在8mL处;
(4)若按照此实验的设想进行,实验可能遇到诸多问题,发生危险,造成实验失败.例如玻璃管发生炸裂(写出一点即可).
分析 本题是测定氧气在空气中的体积分数的实验探究,要把空气中的氧气消耗掉,在本实验中用的是过量的白磷,燃烧后的生成物是固体,不需要占很大的空间.本实验中用的是40mL的玻璃管与实际容积为60mL且润滑性很好的针筒注射器,并且活塞在20mL处,有助于反应结束后计算体积.要使本实验成功,必须注意以下几点:①装置的气密性好;②白磷足量;③必须冷却到室温再读数.还要注意防止玻璃管受热不均或气体体积受热膨胀过大,从而造成玻璃管炸裂.
解答 解:(1)打开弹簧夹,将注射器活塞前沿从20mL刻度处推至15mL刻度处,然后松开手,若活塞仍能返回至20mL刻度处,则说明整个装置都不漏气;
(2)若先夹紧弹簧夹,用酒精灯加热白磷,这时白磷燃烧消耗掉的只是试管内的氧气为40mL×$\frac{1}{5}$=8mL,所以活塞应停在20mL-8mL=12mL的刻度处;
(3)若不使用弹簧夹,用酒精灯加热白磷,白磷实际消耗掉的是试管40mL和注射器内20mL的氧气为(40mL+20mL)×$\frac{1}{5}$=12mL,所以活塞应停在20mL-12mL=8mL的刻度处;
(4)因为白磷燃烧放出大量的热,会使密闭体系内气体压强增大,所以该实验中可能出现的问题有:橡胶塞弹出、玻璃管爆裂、注射器活塞弹出等.
故答案为:玻璃管发生炸裂(答案合理即可).
故答案为:
(1)装置气密性好;
(2)注射器的活塞停在12mL;
(3)注射器的活塞先向右移动,然后停在8mL处;
(4)玻璃管发生炸裂.
点评 本题主要考查实验测定空气中氧气含量的原理及可能造成实验失败的原因的分析,解此类问题时关键是分析清楚实验原理,了解实验过程中的注意事项.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
13.下列图象能正确表示其对应关系的是( )
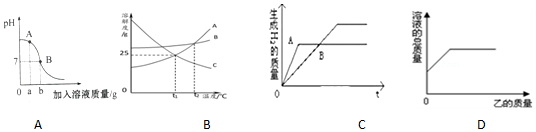

| A. | B点表示稀盐酸和加入NaOH溶液质量一定相同 | |
| B. | t1℃时,A、C物质饱和溶液中溶质的质量分数为25% | |
| C. | 等质量的锌和铁与足量盐酸反应,A为锌B为铁 | |
| D. | 向硫酸铜溶液中加入足量的铁粉,溶液质量的变化 |
14.2016冬季雾霾席卷大半个中国,对空气造成了严重污染.下列做法有利于减少雾霾的是( )
| A. | 大力发展火电 | B. | 露天焚烧秸秆 | C. | 开发清洁能源 | D. | 提倡多开汽车 |
11.某地城际铁路的建成将进一步推动该市经济的发展,在修建铁路的土石方爆破中要用到黑火药,黑火药爆炸时发生反应的化学方程式是2KNO3+3C+S$\frac{\underline{\;点燃\;}}{\;}$K2S+3CO2↑+X↑,根据以上信息,下列说法错误的是( )
| A. | X的化学式是N2 | B. | 黑火药是混合物 | ||
| C. | KNO3中氮元素的化合价为+5价 | D. | 该反应属于化合反应 |
18.为确定某大理石样品的纯度,某兴趣小组进行如下实验:称取该大理石(主要成分是CaCO3;,杂质不参加反应)加入烧杯中,向其中逐渐加入稀盐酸至完全反应.反应结束后,称量烧杯的总质量(溶解的气体忽略不计),有关数据记录如下表.
(1)实验中判断碳酸钙已经完全反应的方法是不再产生气泡.
(2)实验中产生的二氧化碳质量为3.3克,该大理石样品的纯度是88.2%.(计算结果精确到0.1%)
(3)实验中若用浓盐酸代替稀盐酸,会使实验结果偏大,原因是什么?浓盐酸易挥发,挥发后导致计算的二氧化碳质量偏大,从而导致计算的碳酸钙质量分数偏大.
(4)大理石是重要的建筑材料,在实际应用中应避免与酸接触.
| 烧杯 | 大理石 | 稀盐酸 | 反应后烧杯及其中物质总质量 | |
| 质量(克) | 90 | 8.5 | 50 | 145.2 |
(2)实验中产生的二氧化碳质量为3.3克,该大理石样品的纯度是88.2%.(计算结果精确到0.1%)
(3)实验中若用浓盐酸代替稀盐酸,会使实验结果偏大,原因是什么?浓盐酸易挥发,挥发后导致计算的二氧化碳质量偏大,从而导致计算的碳酸钙质量分数偏大.
(4)大理石是重要的建筑材料,在实际应用中应避免与酸接触.
13.如表是100g某品牌板栗的部分营养成分.
(1)食物的成分主要有七大类营养素,上表中为人体提供主要的能量来源的是糖类.
(2)假设该板栗中的钠元素以氯化钠的形式存在,则100g该板栗中,氯化钠的质量是多少?
| 总热量 | 蛋白质 | 糖类 | 油脂 | 钠 | 维生素C |
| 1016kJ | 5.1g | 11.3g | 19g | 4.6mg | 3.3mg |
(2)假设该板栗中的钠元素以氯化钠的形式存在,则100g该板栗中,氯化钠的质量是多少?