题目内容
为测定某CuSO4溶液的溶质质量分数。化学小组的同学取CuSO4溶液100g,向其中滴加一定浓度的NaOH溶液,至不再产生沉淀为止,共用去NaOH溶液80g,过滤,得到滤液175.1g。请计算:
(1)该反应生成沉淀_____g;
(2)该硫酸铜溶液的溶质质量分数。
(温馨提示:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4)
【答案】(1)4.9
(2)设100g CuSO4溶液中所含CuSO4质量为x
CuSO4+2NaOH═Na2SO4+Cu(OH)2↓
160 98
x 4.9g
160:98=x:4.9g
x=8g
CuSO4溶液中溶质的质量分数=8g/100g×100%=8%
答:CuSO4溶液中溶质的质量分数=8g/100g×100%=8%。
【解析】(1)根据质量守恒定律求出沉淀的质量,反应生成沉淀的质量为100g+80g-175.1g=4.9g;(2)根据化学反应方程式列式计算,根据生成Cu(OH)2沉淀的质量可求出参加反应的CuSO4质量,进而可求出CuSO4溶液中溶质的质量分数。

练习册系列答案
相关题目
为了测定某纯碱样品(含少量氯化钠杂质)中碳酸钠的质量分数,取该样品与足量稀盐酸在烧杯中反应,有关实验数据如下表
| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸的质量/g | 纯碱样品的质量/g | 烧杯和其中混合物的质量/g |
| 120 | 12 | 127.6 |
请计算:
(1)反应生成二氧化碳的质量为 g。
(2)该纯碱样品中碳酸钠的质量分数为多少。(请写出计算过程)

 生装置中制取氢气,实验过程中,首级到的氢气与反应时间关系如图所示,求反应后所得硫酸锌溶液的溶质质量分数。
生装置中制取氢气,实验过程中,首级到的氢气与反应时间关系如图所示,求反应后所得硫酸锌溶液的溶质质量分数。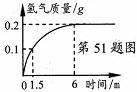
 。
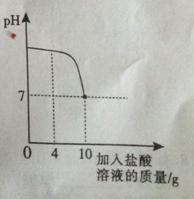
。 含量,取10g水垢样品,向样品中加入足量的稀盐酸,其变化关系如下图所示,试计算:
含量,取10g水垢样品,向样品中加入足量的稀盐酸,其变化关系如下图所示,试计算:
 B.②③④ C.③④⑤ D.②③⑤
B.②③④ C.③④⑤ D.②③⑤