题目内容
13.现有一定量的氯化钠废液,可能含有碳酸钠、硫酸钠、氢氧化钠中的一种或几种.星光学习小组探究其组成成分,并除去其中的杂质,得到氯化钠溶液.他们设计如下实验方案:步骤一:取适量的氯化钠废液,加入过量的氯化钡溶液,发现有白色沉淀生成.过滤,得到白色沉淀A和无色滤液B.
分析一:白色沉淀A可能含有碳酸钡、硫酸钡(填化学式).写出可能发生反应的一个化学方程式:BaCl2+Na2CO3═BaCO3↓+2NaCl或BaCl2+Na2SO4═BaSO4↓+2NaCl.
步骤二:向白色沉淀A滴加足量的稀硝酸,观察到的现象有气泡产生,沉淀部分溶解
分析二:这种氯化钠废液中一定含有的溶质Na2CO3、Na2SO4(填化学式).
步骤三:取少量无色滤液B,滴加酚酞溶液,观察到的现象溶液变红
分析三:这种氯化钠废液中一定还含有的溶质NaOH(填化学式).
结 论:这种氯化钠废液中含有碳酸钠、硫酸钠、氢氧化钠.
步骤四:向无色滤液B中加入的Na2CO3(填化学式)溶液,过滤,得到白色沉淀C和无色滤液D.
分析四:此步骤操作的实验目的是除去过量的氯化钡
步骤五:向无色滤液D中逐滴加入HCl(填化学式)溶液,直到溶液的pH等于(填“大于”“等于”“小于”)7为止,得到氯化钠溶液.
分析五:此步骤操作的实验目的是除去过量的碳酸钠
反 思:步骤一中加入过量的氯化钡溶液的目的是将碳酸钠和硫酸钠全部除去.
分析 根据已有的物质的性质以及性质差异和物质间反应的实验现象进行分析解答即可.
解答 解:现有一定量的氯化钠废液,可能含有碳酸钠、硫酸钠、氢氧化钠中的一种或几种.星光学习小组探究其组成成分,并除去其中的杂质,得到氯化钠溶液.他们设计如下实验方案:
步骤一:取适量的氯化钠废液,加入过量的氯化钡溶液,发现有白色沉淀生成.过滤,得到白色沉淀A和无色滤液B,氯化钡能与碳酸钠反应生成碳酸钡沉淀,硫酸钠能与氯化钡反应生成硫酸钡沉淀,故得到的白色沉淀A可能含有碳酸钡和硫酸钡,故填:碳酸钡、硫酸钡,BaCl2+Na2CO3═BaCO3↓+2NaCl或BaCl2+Na2SO4═BaSO4↓+2NaCl.
步骤二:向白色沉淀A滴加足量的稀硝酸由于结论是含有碳和硫酸钠,故会观察到沉淀部分溶解,有气泡产生,故填:有气泡产生,沉淀部分溶解;
分析二:这种氯化钠废液中一定含有的溶质碳酸钠和硫酸钠,故填:Na2CO3、Na2SO4;
步骤三:由于结论中含有氢氧化钠,故取少量无色滤液B,滴加酚酞试液溶液,观察到酚酞变红的现象,故填:酚酞,溶液变红;
分析三:这种氯化钠废液中一定还含有的溶质氢氧化钠,故填:NaOH;
步骤四:为了得到氯化钠,需要将其中含有的过量的氯化钡除去,故向无色滤液B中加入的碳酸钠溶液,过滤,得到白色沉淀C和无色滤液D,故填:Na2CO3.
分析四:加入过量的碳酸钠溶液的实验目的是除去过量的氯化钡溶液,故填:除去过量的氯化钡;
步骤五:加入过量的碳酸钠引入了新的杂质,需要向无色滤液D中逐滴加入稀盐酸溶液,直到溶液的pH等于7为止,得到氯化钠溶液,故填:HCl,等于.
分析五:加入盐酸的实验目的是除去过量的碳酸钠,故填:除去过量的碳酸钠;
反 思:步骤一中加入过量的氯化钡溶液的目的是将碳酸钠和硫酸钠全部除去,故填:将碳酸钠和硫酸钠全部除去.
点评 本题考查的是常见的物质的成分的推断以及物质的除杂的知识,完成此题,可以依据已有的知识进行.

 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案| A. | 能否保持物质的化学性质 | B. | 质量和体积的大小不同 | ||
| C. | 运动形式和间隔的远近不同 | D. | 在化学反应里是否可分 |
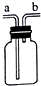 如图装置既可以用于排空气法又可以用于排水法收集气体.无论瓶内装满空气还是装满水,收集气体时,制的气体都从b端进入,该气体是( )
如图装置既可以用于排空气法又可以用于排水法收集气体.无论瓶内装满空气还是装满水,收集气体时,制的气体都从b端进入,该气体是( )| A. | O2 | B. | CO2 | C. | H2 | D. | CO |