题目内容
KClO3和MnO2混合物中经测定MnO2质量分数为15%,加热一段时间后冷却至室温,测得MnO2质量分数为18.5%,请计算KClO3分解的百分率是多少?
答案:
解析:
解析:
|
解答:设反应前混合物的质量为100g,则KClO3质量为85g、MnO2质量为15g.根据催化剂反应前后质量不变的性质计算: 反应后混合物质量:15g÷18.5%=81.08g因此产生的O2质量:100g-81.08g=18.92g 设分解KClO3质量为x 2KClO3 2×122.5 3×32 x 18.92g KClO3分解的百分率为: |

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
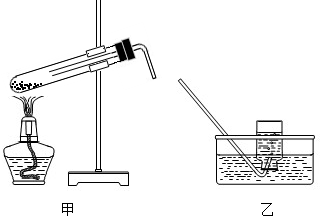 某生欲按右图装置制取氧气(所用药品为KClO3和MnO2).
某生欲按右图装置制取氧气(所用药品为KClO3和MnO2).
