题目内容
 水是宝贵的自然资源.
水是宝贵的自然资源.①活性炭常用于净水,利用其
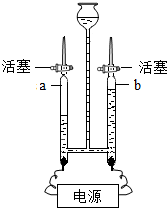
②电解水实验如图所示.
Ⅰ.a管下方导线应接电源的
Ⅱ.为了加快电解速度,可先向水里加入少量氢氧化钠(已知通电时NaOH不发生变化).配制100g溶质质量分数为10%的氢氧化钠溶液,需氢氧化钠固体
Ⅲ.水曾被误认为是一种单质.下列实验能证明水是由氢、氧元素组成的是
A.水的电解 B.水的蒸发 C.水的蒸馏 D.氢气在氧气中燃烧.
考点:碳单质的物理性质及用途,电解水实验,书写化学方程式、文字表达式、电离方程式
专题:空气与水
分析:①根据活性炭常由吸附性分析回答.
②Ⅰ.根据电解水的现象和反应分析回答.
Ⅱ.根据溶质质量分数的定义、配置分析回答;
Ⅲ.根据质量守恒定律分析判断.
②Ⅰ.根据电解水的现象和反应分析回答.
Ⅱ.根据溶质质量分数的定义、配置分析回答;
Ⅲ.根据质量守恒定律分析判断.
解答:解:①由于活性炭由吸附性,在活性炭常用于净水,利用其吸附作用除去水中的颜色和异味.
②Ⅰ.由电解水实验图可知,a管收集的气体较多是氢气,a管下方导线应接电源的负极,反应的化学方程式为2H2O
2H2↑+O2↑.
Ⅱ.配制100g溶质质量分数为10%的氢氧化钠溶液,需氢氧化钠固体是:100g×10%=10g,需要水是90g,体积为90mL,量取水(水的密度为1g/cm3)时,应选择规格为100mL的量筒.电解后由于水的质量减少了,所以,溶液的溶质质量分数>10%.
Ⅲ.A、水通电可以分解出氢气和氧气,正极产生氧气、负极产生氢气,二者气体体积之比为1:2;组成氢气的氢元素、氧气的氧元素都来自水,所以水是由氢、氧两种元素组成的,能判断水的组成.
B、水的蒸发是液态的水变为气态水的过程,发生物理变化,无法判断水的组成.
C、水的蒸馏是除去水中可溶的物质的操作,无法判断水的组成;
D、氢气燃烧生成水,氢气是由氢元素组成的,氧气是由氧元素组成的,由化学反应前后元素种类不变,可以得出水是由氢、氧两种元素组成的,能判断水的组成.
故答为:①吸附.②Ⅰ.负,2H2O
2H2↑+O2↑.Ⅱ.10g,100,>.Ⅲ.AD.
②Ⅰ.由电解水实验图可知,a管收集的气体较多是氢气,a管下方导线应接电源的负极,反应的化学方程式为2H2O
| ||
Ⅱ.配制100g溶质质量分数为10%的氢氧化钠溶液,需氢氧化钠固体是:100g×10%=10g,需要水是90g,体积为90mL,量取水(水的密度为1g/cm3)时,应选择规格为100mL的量筒.电解后由于水的质量减少了,所以,溶液的溶质质量分数>10%.
Ⅲ.A、水通电可以分解出氢气和氧气,正极产生氧气、负极产生氢气,二者气体体积之比为1:2;组成氢气的氢元素、氧气的氧元素都来自水,所以水是由氢、氧两种元素组成的,能判断水的组成.
B、水的蒸发是液态的水变为气态水的过程,发生物理变化,无法判断水的组成.
C、水的蒸馏是除去水中可溶的物质的操作,无法判断水的组成;
D、氢气燃烧生成水,氢气是由氢元素组成的,氧气是由氧元素组成的,由化学反应前后元素种类不变,可以得出水是由氢、氧两种元素组成的,能判断水的组成.
故答为:①吸附.②Ⅰ.负,2H2O
| ||
点评:本题考查了水的有关知识,属于课本的基础知识,完成此题,可以依据已有的知识进行.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
下列粒子结构示意图中,表示阴离子的是( )
A、 |
B、 |
C、 |
D、 |
同学们填写的“毕业生登记表”需要长期保存,因此书写时必须使用( )
| A、碳素笔 | B、圆珠笔 |
| C、红墨水笔 | D、铅笔 |
下列现象或事实,用相关知识解释不正确的是( )
| A、10mL水与10mL酒精混合,所得液体体积小于20mL--分子发生了变化 |
| B、氧化汞受热分解生成汞和氧气--在化学变化中分子可分,原子不可分 |
| C、品红在水中扩散--分子在不停运动 |
| D、热胀冷缩现象--分子间有间隙 |
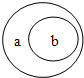 概念之间具有并列、包含、交叉等关系.下列选项中所列概念之间的关系,符合图中a、b所示包含关系的是( )
概念之间具有并列、包含、交叉等关系.下列选项中所列概念之间的关系,符合图中a、b所示包含关系的是( )| A、化合物、氧化物 |
| B、纯净物、混合物 |
| C、单质、化合物 |
| D、氧化反应、化合反应 |
某同学实验时记录的现象,其中正确的是( )
| A、红磷在空气中燃烧,产生大量白色烟雾 |
| B、硫在氧气中燃烧,产生微弱的淡蓝色火焰 |
| C、硫酸铜溶液中滴加氢氧化钠溶液,产生白色沉淀 |
| D、向滴有酚酞的氢氧化钠溶液中不断滴加盐酸,溶液由红色逐渐变成无色 |
