题目内容
6.5克锌与100克稀硫酸混合,得到无色溶液。
(1)若二者恰好完全反应,则在100克稀硫酸中溶质的化学式为 ,其质量为  g,溶剂的的化学式为
g,溶剂的的化学式为  ,其质量为 g,完全反应后,所得溶液的质量为 g,其中溶质的化学式为 ,其质量为 g,溶剂的的化学式为 ,其质量为 g。
,其质量为 g,完全反应后,所得溶液的质量为 g,其中溶质的化学式为 ,其质量为 g,溶剂的的化学式为 ,其质量为 g。
(2)若锌完全反应,则所得溶液中溶质的化学式为 。
答案:(1)H2SO4 9.8 H2O 90.2 106.3 ZnSO4 16.1 H2O 90.2
(2)ZnSO4 或ZnSO4和H2SO4
解析:,稀硫酸是溶液,其中的溶质是硫酸,溶剂是水,锌与硫酸反应,与水不反应。根据化学方程式计算相关物质的质量。
Zn + H2SO4 = ZnSO4 + H2↑
65 98 161 2
6.5g x y z
解得: x=9.8g y= 16.1g z= 0.2g
故100g稀硫酸中溶质H2SO4的质量为 9.8g,溶剂水的质量为 100g-9.8g=90 .2g
.2g
根据质量守恒定律,反应后所得溶液质量为 6.5g+100g-0.2g=106.3g,其中溶质为ZnSO4 的质量为16.1g,溶剂质量的质量不变,为 90.2g。

下列做法,对保护环境不利的是( )
|
| A. | 开发推广氢能汽车 | B. | 汽车限购限行 |
|
| C. | 燃放烟花爆竹增强节日气氛 | D. | 用天然气代替燃煤供暖 |
除去下列物质中所含杂质(括号内为杂质),所选用试剂及操作方法均正确的一组是( )
| 选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
| A | NaOH(Na2CO3) | 氯化钙溶液 | 溶解、过滤、蒸发、结晶 |
| B | CO2(CO) | 氧气 | 点燃 |
| C | Cu(CuO) | 稀盐酸 | 溶解、过滤、洗涤、干燥 |
| D | CuSO4(H2SO4) | 氢氧化钠溶液 | 过滤 |
 C.稀盐酸 D.水
C.稀盐酸 D.水  应可得到B,
应可得到B, 则C与D反应的化学方程式
则C与D反应的化学方程式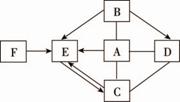 (4)已知上述物质间存在右图所示的关系
(4)已知上述物质间存在右图所示的关系 ①浓硫酸和水 ②镁和稀盐酸
①浓硫酸和水 ②镁和稀盐酸 氧化钠固体和水 ⑥碳酸氢钠和稀盐酸
氧化钠固体和水 ⑥碳酸氢钠和稀盐酸



 C D
C D D. 撤离可燃物
D. 撤离可燃物