题目内容
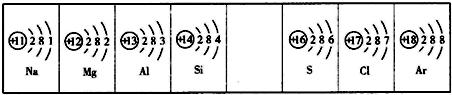
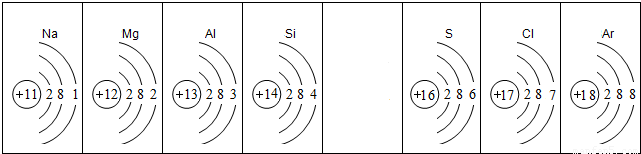
下列是部分元素的原子结构示意图、主要化合价等信息.请完成下列填空:
| 第二周期 | 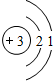 锂 锂 | 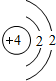 铍 铍 | 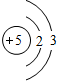 硼 硼 | 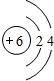 碳 碳 | 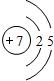 氮 氮 | 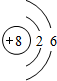 氧 氧 | 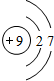 氟 氟 |
| 主要 化合价 | +1 | +2 | +3 | +4,-4 | +5,-3 | -2 | -1 |
| 第三周期 | 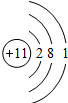 钠 钠 | 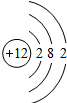 镁 镁 | 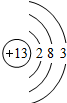 铝 铝 | 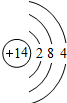 硅 硅 | 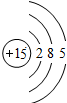 磷 磷 | 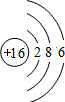 硫 硫 | 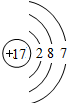 氯 氯 |
| 主要 化合价 | +1 | +2 | +3 | +4,-4 | +5,-3 | +6,-2 | +7,-1 |
(2)根据此表信息可以总结很多有规律性的知识:①元素的最高正价与原子的______相等;②同一周期元素的原子的______相等.
解:(1)根据题目的表中看到,原子序数为8的元素是氧元素,化合价为-2价;原子序数为14的元素是硅元素,化合价为+4、-4价.硅和氧结合硅显+4价,化合物为SiO2;
(2)从表中给出的每周期元素的原子结构示意图和化合价可看出,原子结构和元素化合价的关系是:最外层电子数=正化合价数,负化合价数=8-最外层电子数;原子结构和周期数的关系是:周期数=电子层数.
故答案为:(1)SiO2;
(2)最外层电子数,电子层数.
分析:(1)根据两种元素的化合价可以写出其组成化合物的化学式;
(2)从题目表中给出的每周期元素的原子结构示意图和化合价可判断出之间的关系.
点评:本题主要考查原子结构示意图、根据化合价书写化学式以及原子结构与化合价、周期数的关系.
(2)从表中给出的每周期元素的原子结构示意图和化合价可看出,原子结构和元素化合价的关系是:最外层电子数=正化合价数,负化合价数=8-最外层电子数;原子结构和周期数的关系是:周期数=电子层数.
故答案为:(1)SiO2;
(2)最外层电子数,电子层数.
分析:(1)根据两种元素的化合价可以写出其组成化合物的化学式;
(2)从题目表中给出的每周期元素的原子结构示意图和化合价可判断出之间的关系.
点评:本题主要考查原子结构示意图、根据化合价书写化学式以及原子结构与化合价、周期数的关系.

练习册系列答案
相关题目