题目内容
17.(1)下列关于氢氧化钡性质的描述中,不属于碱的共同性质的是C.A.能使紫色石蕊溶液变蓝色 B.能与盐酸反应生成水
C.能与Na2CO3溶液反应生成沉淀 D.能与CO2反应生成水
(2)碱能表现出一些共同的性质,这是因为碱溶液中都含有OH-(用符号表示).
(3)根据图可以看出酸与碱发生中和反应的微观本质是H++OH-═H2O(或氢离子和氢氧化根离子结合生成水).

(4)请写出氢氧化钡与下列物质反应的化学方程式:
①与CO2反应Ba(OH)2+CO2═BaCO3↓+H2O;②与Na2SO4溶液反应Ba(OH)2+Na2SO4═BaSO4↓+2NaOH.
分析 (1)A、根据碱与能跟酸碱指示剂作用判断;B、根据盐酸能发生中和反应判断;C、根据生成的沉淀是钡离子和硫酸根离子作用的结果分析;D、碱能和非金属氧化物反应判断;
(2)碱具有共性是因为溶液中含有相同的阴离子;
(3)酸与碱发生中和反应的微观本质是酸中的氢离子与碱中的氢氧根离子结合成水分子;
(4)根据反应物和生成物写出有关反应的化学方程式.
解答 解:(1)A、Ba(OH)2能使紫色石蕊溶液变蓝色,是OH-作用,属于碱的共同性质,故A正确;B、Ba(OH)2与盐酸发生属于酸碱的中和反应,是OH-与氢离子的作用,是碱的共同性质,故B正确;C、Ba(OH)2能与Na2CO3溶液反应生成BaCO3沉淀,是钡离子和碳酸根离子作用的结果,与OH-无关,故C错误;D、Ba(OH)2能与CO2反应生成属于碱和非金属氧化物,属于碱的共同性质,故D正确;故选:C.
(2)碱具有共性是因为溶液中含有相同的阴离子氢氧根离子,故填:OH-;
(3)酸与碱发生中和反应的微观本质是酸中的氢离子与碱中的氢氧根离子结合成水分子,故填:H++OH-═H2O(或氢离子和氢氧根离子结合成水);
(4)①氢氧化钡能与二氧化碳反应生成碳酸钡沉淀和水,故填:Ba(OH)2+CO2═BaCO3↓+H2O;
②氢氧化钡能与氯化铜反应生成氯化钡和氢氧化铜沉淀,故填:Ba(OH)2+CuCl2═BaCl2+Cu(OH)2↓.
点评 本题考查了常见碱的性质,完成此题,可以依据已有的知识进行.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案
相关题目
7.下列说法或做法正确的是( )
| A. | 将稀硫酸和食盐水混合,两者在溶液中不能共存 | |
| B. | 将氢氧化钠溶液和硫酸铜溶液混合,完全反应后所得溶液质量变大 | |
| C. | 公路上的积雪可以用食盐来消除 | |
| D. | 汽车用铅蓄电池中含有盐酸 |
8.下列实验操作中,正确的是( )
| A. |  倾倒液体 | B. |  读取液体的体积 | C. |  塞进橡胶塞 | D. | 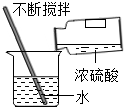 稀释浓硫酸 |
5.玻璃仪器常附着难清洗的物质,下列清洗方法不可行的是( )
| A. | 内壁有碘的试管用酒精清洗 | |
| B. | 内壁有碳酸钙的试管用稀盐酸清洗 | |
| C. | 内壁有植物油的试管用热纯碱溶液清洗 | |
| D. | 内壁有氧化铁的试管用氢氧化钠溶液清洗 |
12.下列关于碳及其化合物的说法,正确的是( )
| A. | 二氧化碳是导致酸雨的主要气体 | |
| B. | 可以用燃烧法除去二氧化碳中混有的少量一氧化碳 | |
| C. | 中国古代字画经久不褪色,因为常温下碳的化学性质不活泼 | |
| D. | CO和CO2都是非金属氧化物,都能与NaOH溶液反应 |
2.下列有关物质的用途,利用了物理性质的是( )
| A. | 铜丝用作电线 | B. | 用氢气作燃料 | ||
| C. | 一氧化碳用于炼铁 | D. | 用稀硫酸除去铁锈 |
6.下列关于微观粒子的叙述,错误的是( )
| A. | 在原子中,质子数不一定等于核外电子数 | |
| B. | 核外电子数在化学反应中经常充当重要的角色 | |
| C. | 化学反应前后原子的种类、数目均保持不变 | |
| D. | 量体温时,温度计中汞原子间的空隙增大 |
7.课外小组同学利用如图所示装置进行实验.实验开始抢红墨水左右两端液面保持相平,容器Ⅰ、Ⅱ体积相同,试验时将针筒内全部液体同时迅速注入容器中.实验内容如表所示
(1)实验前,用手紧握容器Ⅰ,一段时间后观察到红墨水液面左低右高,松手后,对容器Ⅱ重复以上操作,观察到红墨水液面左高右低,以上实验说明气密性好(选填“好”或“差”)
(2)实验b的现象容器Ⅰ中石灰水变浑浊,红墨水左低右高
(3)实验c,针筒I、Ⅱ内盐酸足量且溶质质量分数相同,红墨水的液面位置是左低右高,产生此现象的原因是等质量的镁、铝与足量盐酸反应,铝生成的氢气多,容器Ⅱ比容器Ⅰ的压强小.

| 实验编号 | 容器Ⅰ | 针筒Ⅰ | 容器Ⅱ | 针筒Ⅱ | 红墨水液面位置 |
| a | 生石灰 | 10mL水 | NaCl | 10mL水 | 保持左低右高 |
| b | 二氧化碳(充满) | 10mL澄清石灰水 | 二氧化碳(充满) | 10mL浓氢氧化钠溶液 | |
| c | 1g铝 | 15mL盐酸 | 1g镁 | 15mL盐酸 |
(2)实验b的现象容器Ⅰ中石灰水变浑浊,红墨水左低右高
(3)实验c,针筒I、Ⅱ内盐酸足量且溶质质量分数相同,红墨水的液面位置是左低右高,产生此现象的原因是等质量的镁、铝与足量盐酸反应,铝生成的氢气多,容器Ⅱ比容器Ⅰ的压强小.