题目内容
6.金属M与AgNO3溶液反应的方程式为:M+2AgNO3═M(NO3)2+2Ag.说法错误的是( )| A. | M的金属活动性比Ag强 | B. | 金属M可能是铜 | ||
| C. | 金属M可能是铝 | D. | 该反应前后M的化合价发生了改变 |
分析 根据题意,金属M能与硝酸银反应置换出银,说明R的活动性比银强,再结合反应的方程式进行有关问题的分析判断.
解答 解:A、由于金属M能与硝酸银反应置换出银,说明M的金属活动性比银强,故说法正确;
B、由于铜的金属活动性比Ag强,金属M可能是铜,并且铜的化合价为+2价,故说法正确;
C、如果M是铝,铝与硝酸银反应生成银和硝酸铝,由于硝酸根-1价,铝+3价,所以硝酸铝写为:Al(NO3)3,图示中M是+2价,所以M不能是铝,故说法错误;
D、反应前M是单质化合价为0,反应后生成了M(NO3)2,M的化合价是+2价,化合价发生了改变,故说法正确.
故选:C.
点评 金属单质能置换出盐中的金属,说明组成单质的金属元素的活动性比盐中金属元素的活动性强.

练习册系列答案
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
16.市场上有一种“冷敷袋”,其主要成分由水和物质A组成,使用时只要将水和物质A混合,轻轻摇晃,就可作冰袋使用.其中物质A可能是( )
| A. | 氯化钠 | B. | 氢氧化钠 | C. | 硝酸铵 | D. | 浓硫酸 |
17.如图所示的变化中,属于化学变化的是( )
| A. |  干冰的升华 | B. | 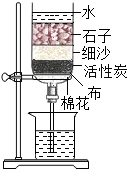 水的净化 | ||
| C. | 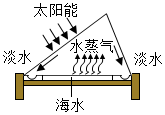 海水的淡化 | D. | 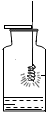 铁丝在氧气中燃烧 |
1.某物质的饱和溶液析出晶体后,下列有关说法正确的是( )
| A. | 溶剂的质量一定变小 | B. | 溶质的质量一定变小 | ||
| C. | 溶质质量分数一定变小 | D. | 溶液的质量可能不变 |
11.在密闭容器内发生化学反应,反应前后各物质质量见表.有关说法错误的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 8 | 32 | 5 | 4 |
| 反应后质量(g) | 16 | 4 | × | 24 |
| A. | 该反应属于分解反应 | |
| B. | 并可能是该反应的催化剂 | |
| C. | 甲乙两物质在反应中的质量比是1:4 | |
| D. | 甲物质可能为单质 |
18.下列说法中正确的是( )
| A. | C、CO、CO2都具有还原性 | |
| B. | 用点燃法可除去CO2中混有的少量的CO | |
| C. | 碳具有可燃性,常温下其化学性质比较活泼 | |
| D. | 用紫色石蕊溶液可区分CO和CO2 |
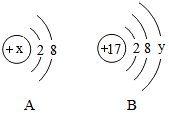 如图中A、B分别是某微粒的结构示意图,根据图示回答下列问题:
如图中A、B分别是某微粒的结构示意图,根据图示回答下列问题: