题目内容
20.实验室有大理石、稀盐酸、澄清的石灰水、紫色石蕊溶液和一种暗紫色的药品,还有下列仪器及棉花、火柴等用品.请回答下列问题:(1)沁馨同学要制备并检验二氧化碳,需要选择的仪器是①②⑦⑧(填序号),还需补充的一种仪器是②长颈漏斗(填名称).
(2)若用图A验证二氧化碳的性质,观察到了预期的现象.产生现象原因是①二氧化碳溶于水且与水反应,消耗瓶内的二氧化碳,使瓶内气体减少,气压减小,小与外界大气压,在压强差的作用下,②塑料瓶变瘪;又因为③二氧化碳与水反应生成碳酸(或CO2+H2O=H2CO3),
碳酸显酸性,使紫色石蕊溶液④变红.
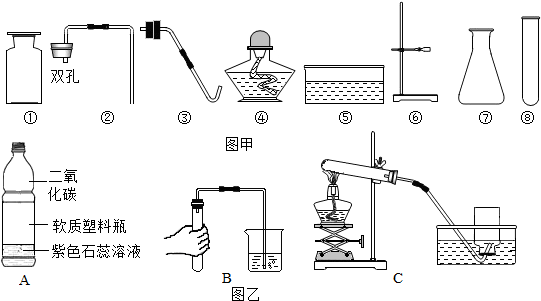
(3)连接仪器装置后,要检查装置的气密性,如图B所示,①用手紧握试管,观察水中的导管口是否有气泡冒出.如果没有气泡冒出,要仔细检查原因,如塞紧橡胶塞或②更换橡皮塞,直至装置不漏气才能进行实验.
(4)写出实验室用一种暗紫色的药品制取氧气的化学方程式①2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;②将实验室用此药品制取氧气的实验装置图C补充完整.
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.图A验证二氧化碳的性质,产生的现象是:塑料瓶变瘪,紫色变红色;因为二氧化碳与水反应生成碳酸(或CO2+H2O=H2CO3),碳酸显酸性;连接仪器装置后,要检查装置的气密性,如图B所示,用手紧握试管,更观察水中的导管口是否有气泡冒出;如果没有气泡冒出,要仔细检查原因,如塞紧橡胶塞或换橡皮塞,直至装置不漏气才能进行实验;
解答 解:(1)要制备并检验二氧化碳,需要选择的仪器是①②⑦⑧;还需补充的一种仪器是长颈漏斗,方便加液体药品,故答案为:②⑦⑧;②长颈漏斗;
(2)图A验证二氧化碳的性质,产生的现象是:塑料瓶变瘪,紫色变红色;因为二氧化碳与水反应生成碳酸(或CO2+H2O=H2CO3),碳酸显酸性;故答案为:①二氧化碳溶于水且与水反应;②塑料瓶变瘪;③二氧化碳与水反应生成碳酸(或CO2+H2O=H2CO3),碳酸显酸性;④变红.
(3)连接仪器装置后,要检查装置的气密性,如图B所示,用手紧握试管,更观察水中的导管口是否有气泡冒出;如果没有气泡冒出,要仔细检查原因,如塞紧橡胶塞或换橡皮塞,直至装置不漏气才能进行实验;故答案为:①用手紧握试管;②更换橡皮塞(或更换胶皮导管等合理即可);
(4)高锰酸钾是暗紫色的,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;如果用高锰酸钾制氧气就需要加热,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集故答案为:①2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;②见右图参照中考的评分标准 (发生装置(1分),收集装置(1分),错一处扣(1分),扣完为止)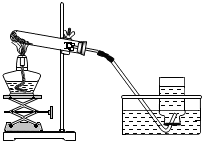
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和气体的性质等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案| A. | Fe(过量)、KNO3、CuSO4 | B. | Fe(过量)、Cu(NO3)2、AgNO3 | ||
| C. | Zn、NaCl、CuCl2(过量) | D. | Cu(过量)、FeCl2、HCl |
【提出问题】该金属丝是什么?它的存在是不是蜡烛灭而复燃的原因?
【初步探究】蜡烛为什么会灭而复燃?
【资料一】蜡烛的棉芯里藏有一些金属,当蜡烛燃烧时,棉芯里的金属被熔化的石蜡包裹起来,由于隔绝了氧气,金属并不燃烧;但当蜡烛熄灭后,金属接触到氧气就可以燃烧,从而使蜡烛复燃.
【实验反思】蜡烛燃烧产生的火焰是由气态(填“固态”或“气态”)物质燃烧产生的,紫琦认为这种蜡烛也可以熄灭,她可以采用的方法是隔绝氧气或剪除灯芯或用湿抹布盖灭.
【资料二】蜡烛内的金属是Mg、Fe或Cu中的一种.
【深入探究】这种蜡烛芯内的金属是Mg、Fe或Cu中的哪一种?
【猜想与假设】(1)根据已有的知识大家一致认为,该金属不可能是Fe和Cu,
其原因是:①铜是紫红色的,不是银白色的;②铁在空气中不能燃烧.
同学们一致猜想:该金属是Mg.
【查阅资料】镁可以与热水反应,生成氢氧化镁,温度越高,水中溶解的氢氧化镁越多.
【进行实验】为了验证猜想,大家设计了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 将该金属丝用砂纸打磨至光亮,加入到装有热水的试管中,并将燃着的小木条放在试管口 | 有气泡不断冒出,气体燃烧,听见爆鸣声,火焰呈淡蓝色 | 生成的气体为_H2 (填化学式) |
| 在反应后的溶液中滴加酚酞溶液 | 溶液变成红色,冷却后红色褪去 | 反应生成了Mg(OH)2,滴加酚酞溶液,溶液变为红色,说明溶液显碱 性 |
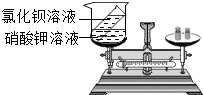 小贝设计如图所示的实验来验证质量守恒定律.将图示中的两种溶液混合前后天平仍然平衡,小贝认为实验成功,你认为小贝的实验设计合理吗?为什么?
小贝设计如图所示的实验来验证质量守恒定律.将图示中的两种溶液混合前后天平仍然平衡,小贝认为实验成功,你认为小贝的实验设计合理吗?为什么?
 通过化学启蒙学习,同学们对组成万物的基本物质有了进一步的了解.
通过化学启蒙学习,同学们对组成万物的基本物质有了进一步的了解.