题目内容
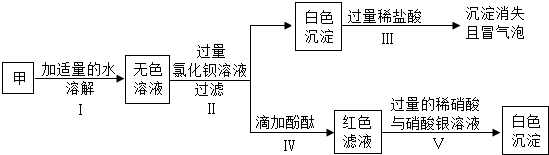
15.某些食品的包装袋内,放有装有白色颗粒状固体的小纸袋,上面写着“干燥剂,主要成分为生石灰”.某同学对一袋久置空气中的干燥剂进行了探究.他先取部分久置干燥剂倒入适量水中,充分搅拌、过滤,得到白色固体和滤液.然后对滤液的酸碱性和白色固体的组成作了探究.
【实验探究一】探究滤液的酸碱性
该同学测定了滤液的酸碱性,你认为该滤液显碱性(或中性)(填“酸性”“碱性”或“中性”).
【实验探究二】探究白色固体的组成
该同学认为白色固体中可能含有的物质是CaO、Ca(OH)2、CaCO3.
他查阅有关资料得知:
CaO是一种白色固体,俗称生石灰,能与水反应生成氢氧化钙,并放出热量.氢氧化钙微溶于水.
【分析判断】你认为该白色固体中一定不含有的物质是氧化钙.
【实验操作】下面是该同学设计的进一步探究白色固体组成的实验方案,请你和他一起完成实验报告.
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量白色固体,倒入适量水,充分搅拌、静置; ②向上层清液中滴加无色酚酞溶液 | 上层清液呈 现红色 | 白色固体中一定含有氢氧化钙 |
| 另取少量白色固体放入试管中,滴加稀盐酸 | 产生气泡 | 白色固体中一定含有碳酸钙 |
(1)只通过以上实验,还不能证明这袋久置于空气中的干燥剂中是否含有CaO.请用化学方程式表示原因CaO+H2O═Ca(OH)2.
(2)请你简述一个证明这袋干燥剂中含有较多量CaO的简易实验:取少量干燥剂于试管中,加入少量水、振荡,触摸试管壁,较热,证明有较多量的氧化钙.
分析 本题考查常见物质的成分的探究方法,解题的关键是熟悉常见物质的化学性质;
氢氧化钙的水溶液显碱性;
久置的干燥剂中加入水时,由于氧化钙能与水发生反应,故过滤后的固体中没有氧化钙;
氢氧化钙的水溶液能使酚酞溶液变红色;
碳酸钙属于碳酸盐,可用稀盐酸检验;
氧化钙能与水反应生成氢氧化钙,也使溶液显碱性;可借助于氧化钙与水反应伴随放热的现象进行检验.
解答 解:【实验探究一】如果久置的干燥剂中含有氧化钙,或含有氢氧化钙,或含有氧化钙和氢氧化钙,倒入适量水中,充分搅拌、过滤后的滤液中含有氢氧化钙,滤液显碱性;如果久置的干燥剂中只含有碳酸钙,倒入适量水中,充分搅拌、过滤后的滤液是水,显中性;由分析可知,该滤液显碱性或显中性.
故填:碱性(或中性).
【分析判断】该白色固体中一定不含有的物质是氧化钙,因为氧化钙能和水反应生成氢氧化钙.
故填:氧化钙.
【实验操作】如果白色固体中含有氢氧化钙,那么上层清液显碱性,呈现红色;
如果白色固体中含有碳酸钙,滴加稀盐酸时会产生气泡.
故填:红;产生气泡.
【总结反思】
(1)氧化钙能与水反应生成氢氧化钙,也使溶液显碱性,氧化钙和水反应的化学方程式为:
CaO+H2O═Ca(OH)2.
故填:CaO+H2O═Ca(OH)2.
(2)证明这袋干燥剂中含有较多量氧化钙的方法是:取少量干燥剂于试管中,加入少量水、振荡,触摸试管壁,较热,证明有较多量的氧化钙.
故填:取少量干燥剂于试管中,加入少量水、振荡,触摸试管壁,较热,证明有较多量的氧化钙.
点评 实验是化学的重要组成部分,正确的实验操作是得出科学结论的前提条件之一,因此要学会设计实验、进行实验、分析实验,为得出正确的结论奠定基础.

练习册系列答案
相关题目
3.市售汽水或啤酒里含有的酸是( )
| A. | 醋酸 | B. | 碳酸 | C. | 盐酸 | D. | 硫酸 |
4.下面是从小明同学学习笔记中摘录出来的一些推理,你认为正确的一句是( )
| A. | 元素原子的最外层电子数达到8个电子时,元素的性质比较稳定,所以氖原子化学性质稳定 | |
| B. | 由同种分子构成的物质是纯净物,所以纯净物一定由同种分子构成 | |
| C. | 氧化物中含有氧元素,所以含有氧元素的物质就是氧化物 | |
| D. | 同种元素的原子具有相同的质子数,所以具有相同质子数两种粒子一定是同种元素 |
5.下表为20℃硫酸溶液的密度和质量分数对应关系表
(1)实验桌上有两个大小相同的试剂瓶,装有等体积(约为500毫升)的两瓶液体,一瓶是98%的硫酸,另一瓶是蒸馏水.现不用任何仪器和试剂,如何用简单的方法来加以鉴别?直接拿起两个试剂瓶感受质量,较重的为浓硫酸,较轻的为水.
(2)现要将98%浓硫酸稀释到为稀硫酸,其操作为把浓硫酸缓缓地沿器壁注入盛有水的烧杯中,同时用玻璃棒不断搅拌.
(3)现有一个大烧杯,其中装有溶质质量分数为40%的硫酸,烧杯中悬浮着一个塑料小球.现往烧杯中逐滴加入一定溶质质量分数的氢氧化钡溶液,直到恰好反应为止,停止滴入氢氧化钡溶液(注:BaSO4不溶于水).
①写出上述反应的化学反应方程式:H2SO4 +Ba(OH)2=2H2O+BaSO4↓
②反应完全后,小球所处的位置是C
A.浮于液面上 B.悬浮于烧杯溶液中 C.沉于烧杯底部
你选择的理由是:当恰好完全反应时,烧杯中的液体只有水,液体密度减小.
| 密度(g/cm3) | 1.01 | 1.14 | 1.30 | 1.50 | 1.73 | 1.84 |
| 溶质质量分数(%) | 1 | 20 | 40 | 60 | 80 | 98 |
(2)现要将98%浓硫酸稀释到为稀硫酸,其操作为把浓硫酸缓缓地沿器壁注入盛有水的烧杯中,同时用玻璃棒不断搅拌.
(3)现有一个大烧杯,其中装有溶质质量分数为40%的硫酸,烧杯中悬浮着一个塑料小球.现往烧杯中逐滴加入一定溶质质量分数的氢氧化钡溶液,直到恰好反应为止,停止滴入氢氧化钡溶液(注:BaSO4不溶于水).
①写出上述反应的化学反应方程式:H2SO4 +Ba(OH)2=2H2O+BaSO4↓
②反应完全后,小球所处的位置是C
A.浮于液面上 B.悬浮于烧杯溶液中 C.沉于烧杯底部
你选择的理由是:当恰好完全反应时,烧杯中的液体只有水,液体密度减小.

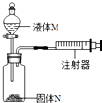 如图所示装置气密性良好、要使注射器中的活塞向右移动,请按要求写出化学方程式:
如图所示装置气密性良好、要使注射器中的活塞向右移动,请按要求写出化学方程式: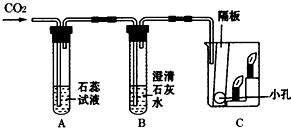 (1)小丽同学设计了右图装置验证二氧化碳的性质,当通入二氧化碳一段时间后,A中发生反应的化学方程为CO2+H2O=H2CO3;B中的现象是澄清石灰水变浑浊;C中观察到蜡烛由低到高依次熄灭,说明二氧化碳的性质有二氧化碳的密度比空气大;不燃烧,不支持燃烧.(答出2条即可).
(1)小丽同学设计了右图装置验证二氧化碳的性质,当通入二氧化碳一段时间后,A中发生反应的化学方程为CO2+H2O=H2CO3;B中的现象是澄清石灰水变浑浊;C中观察到蜡烛由低到高依次熄灭,说明二氧化碳的性质有二氧化碳的密度比空气大;不燃烧,不支持燃烧.(答出2条即可). 如图表示一瓶氯化锌溶液,该溶液由5g固体放入45g水中配制而成.
如图表示一瓶氯化锌溶液,该溶液由5g固体放入45g水中配制而成.