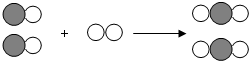题目内容
18.请就如何防止你家的刀、锅、桶等钢铁制品生锈,提出你的建议.分析 铁与氧气和水充分接触时容易生锈,水和氧气同时存在是铁生锈的必要条件;显酸性的溶液、盐溶液能够促进金属生锈.
解答 解:为了防止家里的刀、剪、桶等铁制品生锈,除了保持铁制品干燥外,还有很多其它方法,例如隔绝氧气可以防止铁生锈,在铁制品表面涂油漆、镀一层金属等方法可以使铁制品与氧气隔绝.
故答案为:涂油、保持干燥等.
点评 本题主要考查学生对钢铁锈蚀的条件和如何防护知识的认识.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.2010年4月15日,科学家成功合成了第117号新元素,填补了第116号元素之间的空缺.推测该元素为117号元素的依据是( )
| A. | 中子数 | B. | 质子数 | C. | 电子数 | D. | 中子数和质子数 |
6.在购买和使用化肥时,要了解化肥的性质,以便合理施用,为了给农民做技术指导,小刚利用自己掌握的知识对碳酸钾(K2CO3)、硫酸铵[(NH4)2SO4]两种化肥的相关性质做了以下探究:
【实验探究】完成下列各题
【结论与应用】(5)碳酸钾与硫酸铵不能(填“能”或“不能”)混用,说明原因碳酸钾溶液呈碱性,与硫酸铵混合施用,产生NH3,降低肥效.
【知识拓展】(6)鉴别失去标签的碳酸钾和硫酸铵固体,下列试剂不可能的是C.
A.水 B.稀盐酸 C.氯化钡溶液 D.无色酚酞溶液.
【实验探究】完成下列各题
| 探 究 过 程 | 实 验 现 象 | 结论及化学方程式 | |
| K2CO3 | (NH4)2SO4 | ||
| (1)配制碳酸钾、硫酸铵溶液.分别取碳酸钾和硫酸铵固体,加足量水搅拌. | 得到澄清溶液,温度无明显变化 | 得到澄清溶液,温度明显降低 | 都易溶于水,硫酸铵溶于水时吸收的热量大于放出的热量. |
| (2)猜想与假设. 碳酸钾、硫酸铵溶液的酸碱性都可能有三种情况. 分别取少量两种溶液于两只试管中,滴加紫色石蕊试液. | 变蓝 | 变红 | 说明碳酸钾溶液显碱性; 说明硫酸铵溶液显 酸 性. |
| (3)与盐酸反应. 分别像两只试管中加入稀盐酸. | 有气泡产生 | 无明显现象 | 写出相关的化学方程式2HCl+K2CO3=2=KCl+CO2↑+H2O. |
| (4)与氢氧化钠溶液反应. 分别向两种溶液中加入氢氧化钠溶液. | 无明显现象 | 产生白色沉淀、有刺激性气味的气体生成 | (NH4)2SO4+2NaOH═Na2SO4+2H2O+2NH3↑ |
【知识拓展】(6)鉴别失去标签的碳酸钾和硫酸铵固体,下列试剂不可能的是C.
A.水 B.稀盐酸 C.氯化钡溶液 D.无色酚酞溶液.
3.为测定某BaCl2溶液的溶质质量分数,进行如下实验:取104g该溶液于烧杯中,加入1g稀硝酸溶液酸化,无任何现象,然后将30g一定溶质质量分数的硫酸溶液分三次加入,每次充分反应后过滤、称量(实验中物质的质量损失忽略不计),数据如表:
根据以上数据计算:(BaCl2+H2SO4═BaSO4↓+2HCl)
(1)该实验过程中产生沉淀的总质量为23.3g.
(2)该BaCl2溶液中溶质的质量分数(写出计算过程)
| 第1次 | 第2次 | 第3次 | |
| 加入硫酸溶液的质量/g | 10 | 10 | 10 |
| 过滤后溶液的质量/g | 105 | 105 | 111.7 |
(1)该实验过程中产生沉淀的总质量为23.3g.
(2)该BaCl2溶液中溶质的质量分数(写出计算过程)
10.下列有关说法错误的是( )
| A. | 甲烷是最简单的有机物 | |
| B. | CO能使人中毒,CO2能使澄清石灰水变浑浊 | |
| C. | 铝具有很好的抗腐蚀性是因为其表面生成了致密的氧化铝薄膜 | |
| D. | 水的净化方法中,净化程度最高的是过滤 |

 ”表示氧原子,“
”表示氧原子,“ ”表示碳原子).
”表示碳原子).