题目内容
(2010?黄冈模拟)根据下列要求,写出有关反应的化学方程式(1)实验室制取二氧化碳 ;
(2)工业上制烧碱 ;
(3)有氧化物参加的还原反应 ;
(4)有单质银生成的置换反应 .
【答案】分析:(1)实验室制取二氧化碳的反应物为碳酸钙和盐酸,生成物为氯化钙、水、二氧化碳,则可书写化学方程式;
(2)工业上制烧碱,反应物为碳酸钠、氢氧化钙,生成物为碳酸钙和氢氧化钠,则可书写化学方程式;
(3)有氧化物参加的还原反应,碳还原氧化铜或氧化铁;一氧化碳还原氧化铜和氧化铁,则可书写化学方程式;
(4)有单质银生成的置换反应,可以选择铜与硝酸银反应,此为置换反应,则可书写化学方程式:
解答:解:(1)由题意:反应物为碳酸钙和盐酸,生成物为氯化钙、水、二氧化碳,故化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)由题意:反应物为碳酸钠、氢氧化钙,生成物为碳酸钙和氢氧化钠,故化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+NaOH;
(3)由题意:可以选择一氧化碳还原氧化铜和氧化铁,故化学方程式为Fe2O3+3CO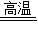 2Fe+3CO2;
2Fe+3CO2;
(4)由题意:可以选择铜与硝酸银反应,此为置换反应,故化学方程式为Cu+2AgNO3=Cu(NO3)2+2Ag
故答为:(1)CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)Na2CO3+Ca(OH)2═CaCO3↓+NaOH;
(3)Fe2O3+3CO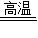 2Fe+3CO2;
2Fe+3CO2;
(4)Cu+2AgNO3=Cu(NO3)2+2Ag
点评:根据题目信息,找出反应物和生成物,再利用书写化学方程式的方法及步骤,根据质量守恒定律,正确书写化学方程式.
(2)工业上制烧碱,反应物为碳酸钠、氢氧化钙,生成物为碳酸钙和氢氧化钠,则可书写化学方程式;
(3)有氧化物参加的还原反应,碳还原氧化铜或氧化铁;一氧化碳还原氧化铜和氧化铁,则可书写化学方程式;
(4)有单质银生成的置换反应,可以选择铜与硝酸银反应,此为置换反应,则可书写化学方程式:
解答:解:(1)由题意:反应物为碳酸钙和盐酸,生成物为氯化钙、水、二氧化碳,故化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)由题意:反应物为碳酸钠、氢氧化钙,生成物为碳酸钙和氢氧化钠,故化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+NaOH;
(3)由题意:可以选择一氧化碳还原氧化铜和氧化铁,故化学方程式为Fe2O3+3CO
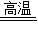 2Fe+3CO2;
2Fe+3CO2;(4)由题意:可以选择铜与硝酸银反应,此为置换反应,故化学方程式为Cu+2AgNO3=Cu(NO3)2+2Ag
故答为:(1)CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)Na2CO3+Ca(OH)2═CaCO3↓+NaOH;
(3)Fe2O3+3CO
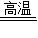 2Fe+3CO2;
2Fe+3CO2;(4)Cu+2AgNO3=Cu(NO3)2+2Ag
点评:根据题目信息,找出反应物和生成物,再利用书写化学方程式的方法及步骤,根据质量守恒定律,正确书写化学方程式.

练习册系列答案
相关题目
(2010?黄冈模拟)钛(Ti)是一种重要的航天金属材料.某学习小组对三种金属Ti、Al、Cu的金属活动性顺序进行探究.过程如下:
【提出假设】A、Ti金属活动性比Al强. B、Al金属活动性比Cu强.
【查阅资料】钛能与盐酸反应.
【实验设计】同温下,取大小相同的这三种金属薄片,分别投入等体积等浓度的足量的稀盐酸中反应,观察现象.
【操作分析】三种金属加入盐酸前都先用砂布将表面擦光亮,其目的是______.
A、除去氧化膜,利于直接反应B、使表面光亮,易观察现象
C、使反应金属温度相同,易反应
【实验现象】
【实验结论】(1)原假设中______不正确(填:“A”、“B”或“A B”).
(2)三种金属的金属活动性由强到弱的顺序为______.
【结论应用】能否用铝制容器来盛装波尔多液(含硫酸铜),______(填“能”或“否”),理由是______.
【提出假设】A、Ti金属活动性比Al强. B、Al金属活动性比Cu强.
【查阅资料】钛能与盐酸反应.
【实验设计】同温下,取大小相同的这三种金属薄片,分别投入等体积等浓度的足量的稀盐酸中反应,观察现象.
【操作分析】三种金属加入盐酸前都先用砂布将表面擦光亮,其目的是______.
A、除去氧化膜,利于直接反应B、使表面光亮,易观察现象
C、使反应金属温度相同,易反应
【实验现象】
| 金属 | Ti | Al | Cu |
| 与盐酸反应现象 | 反应缓慢 | 反应剧烈 | 无明显现象 |
(2)三种金属的金属活动性由强到弱的顺序为______.
【结论应用】能否用铝制容器来盛装波尔多液(含硫酸铜),______(填“能”或“否”),理由是______.
(2010?黄冈模拟)钛(Ti)是一种重要的航天金属材料.某学习小组对三种金属Ti、Al、Cu的金属活动性顺序进行探究.过程如下:
【提出假设】A、Ti金属活动性比Al强. B、Al金属活动性比Cu强.
【查阅资料】钛能与盐酸反应.
【实验设计】同温下,取大小相同的这三种金属薄片,分别投入等体积等浓度的足量的稀盐酸中反应,观察现象.
【操作分析】三种金属加入盐酸前都先用砂布将表面擦光亮,其目的是______.
A、除去氧化膜,利于直接反应B、使表面光亮,易观察现象
C、使反应金属温度相同,易反应
【实验现象】
【实验结论】(1)原假设中______不正确(填:“A”、“B”或“A B”).
(2)三种金属的金属活动性由强到弱的顺序为______.
【结论应用】能否用铝制容器来盛装波尔多液(含硫酸铜),______(填“能”或“否”),理由是______.
【提出假设】A、Ti金属活动性比Al强. B、Al金属活动性比Cu强.
【查阅资料】钛能与盐酸反应.
【实验设计】同温下,取大小相同的这三种金属薄片,分别投入等体积等浓度的足量的稀盐酸中反应,观察现象.
【操作分析】三种金属加入盐酸前都先用砂布将表面擦光亮,其目的是______.
A、除去氧化膜,利于直接反应B、使表面光亮,易观察现象
C、使反应金属温度相同,易反应
【实验现象】
| 金属 | Ti | Al | Cu |
| 与盐酸反应现象 | 反应缓慢 | 反应剧烈 | 无明显现象 |
(2)三种金属的金属活动性由强到弱的顺序为______.
【结论应用】能否用铝制容器来盛装波尔多液(含硫酸铜),______(填“能”或“否”),理由是______.
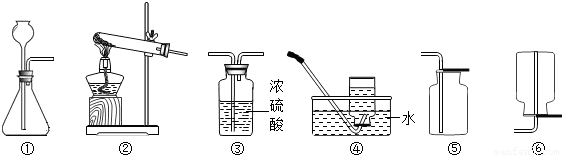
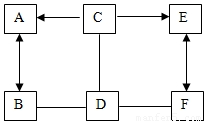
 ”表示两种物质可以互相转化.在通常情况下,E为液体,其余都是气体.试回答下列问题:
”表示两种物质可以互相转化.在通常情况下,E为液体,其余都是气体.试回答下列问题: