题目内容
2.3g某有机物在O2中完全燃烧,生成4.4gCO2和2.7gH2O.该有机物中( )
分析:根据质量守恒定律进行分析,由题意“2.3g某有机物在足量氧气中充分燃烧,生成4.4gCO2和2.7gH2O”,则可计算出4.4gCO2和2.7gH2O中的碳元素和氢元素的质量,碳元素和氧元素完全来自有机物,通过和有机物的质量进行比较,则可推测有机物是否含有氧元素,如果等于有机物的质量,就说明有机物中只含有碳元素和氢元素;如果小于有机物的质量,说明有机物中含有碳、氢、氧三种元素
解答:解:由题意“2.3g某有机物在足量氧气中充分燃烧,生成4.4gCO2和2.7gH2O”,则二氧化碳中碳元素的质量:4.4g×
=1.2g;5.4g水中氢元素的质量为:2.7g×
=0.3g.碳元素和氢元素的质量之和为1.2g+0.3g=1.5g<2.3g,根据质量守恒定律可得有机物中含有碳、氢、氧三种元素.
故选C.
| 12 |
| 44 |
| 2 |
| 18 |
故选C.
点评:根据质量守恒定律的元素守恒的思想,进行计算;培养学生由题目中的信息寻找有价值的条件的能力.

练习册系列答案
相关题目
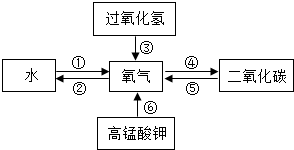 构建知识网络是一种重要的学习方法.如图是某同学构建的有关氧气获得和性质的网络图.请根据题图回答有关问题:
构建知识网络是一种重要的学习方法.如图是某同学构建的有关氧气获得和性质的网络图.请根据题图回答有关问题: