题目内容
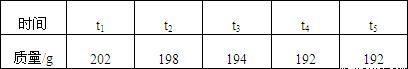
 某同学欲测定一瓶过氧化氢溶液中溶质的质量分数.他把一个质量为30g的烧杯置于电子天平上,慢慢向烧杯中倒入这种过氧化氢溶液,当读数刚好为200g时便停止倒入,然后将8g二氧化锰加入烧杯中.不同时间从电子天平的读数记录如下表.
某同学欲测定一瓶过氧化氢溶液中溶质的质量分数.他把一个质量为30g的烧杯置于电子天平上,慢慢向烧杯中倒入这种过氧化氢溶液,当读数刚好为200g时便停止倒入,然后将8g二氧化锰加入烧杯中.不同时间从电子天平的读数记录如下表.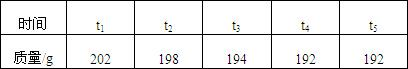
(1)该同学一共制得氧气
(2)这瓶过氧化氢溶液中溶质的质量分数是多少?
分析:(1)根据质量守恒定律解出氧气的质量;
(2)根据求出的氧气的质量利用方程式中的比例关系解出纯净的过氧化氢的质量,
(2)根据求出的氧气的质量利用方程式中的比例关系解出纯净的过氧化氢的质量,
解答:解:反应前烧杯、过氧化氢溶液、二氧化锰的质量总和是208克,反应一段时间后的总质量减少到192克,生成氧气的质量为:208-192=16克,
过氧化氢溶液的质量是200-30=170g,
设生成16克的氧气需要纯净的过氧化氢的质量是X,
2H2O2
2H2O+O2↑
68 32
X 16g
=
X=34g,
所以过氧化氢溶液的质量分数为:
×100%=20%,
故答案为:16g,20%.
过氧化氢溶液的质量是200-30=170g,
设生成16克的氧气需要纯净的过氧化氢的质量是X,
2H2O2
| ||
68 32
X 16g
| 68 |
| X |
| 32 |
| 16g |
X=34g,
所以过氧化氢溶液的质量分数为:
| 34 |
| 170 |
故答案为:16g,20%.
点评:在解此类题时,首先利用质量守恒定律解出氧气的质量,然后利用方程式中的比例关系解出需要求解的物质的质量.

练习册系列答案
相关题目