题目内容
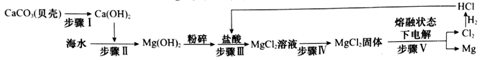
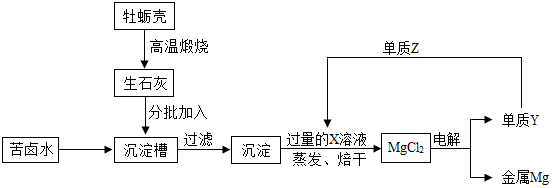
15.海洋中蕴藏着丰富的资源.海水晒盐得到粗盐,剩余的母液称为苦卤,粗盐和苦卤用途也比较广泛.(1)工业上制得金属镁方法:在苦卤(含氯化镁)中加入石灰乳,过滤;在氢氧化镁中加入盐酸,结晶;电解熔融氯化镁制得金属镁.
①上述过程涉及反应的基本类型不包括ac.
a、化合反应 b、分解反应 c、置换反应 d、复分解反应
②加入石灰乳发生反应的化学方程式为MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2.
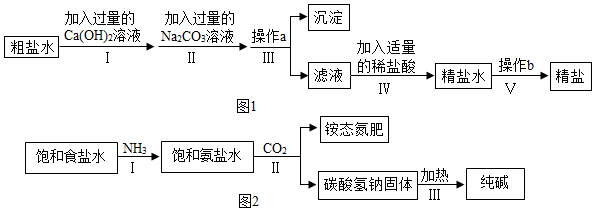
(2)粗盐水常含有MgCl2、CaCl2等杂质,工业粗盐的提纯流程如图1所示.
①如果将Ⅰ和Ⅱ的顺序颠倒,则所制得的精盐水中的溶质有氯化钠、氯化钙.
②操作a、b均用到玻璃棒,其在操作b中的作用是什么?
③写出Ⅳ中盐酸的作用是什么?
(3)采用氨碱法生产纯碱,主要流程如图2.
①上述Ⅰ、Ⅱ两个步骤总反应的化学方程式是NaCl+H2O+CO2+NH3═NaHCO3↓+NH4Cl.
②请简述鉴别铵态氮肥和尿素两种化肥的方法.
(4)现有10t贝壳(主要成分是碳酸钙)煅烧后质量减少了2.2t,可制得氧化钙的质量是多少?(假设其他成分不参加反应).
分析 (1)氯化镁和氢氧化钙反应生成氢氧化镁沉淀和氯化钙,氢氧化镁和稀盐酸反应生成氯化镁和水,电解氯化镁生成镁和氯气;
(2)氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠;
玻璃棒用途有搅拌、引流、转移物质等;
(3)氯化钠、水、氨气、二氧化碳等物质反应生成碳酸氢钠和氯化铵;
铵态氮肥能和碱反应生成氨气,氨气有刺激性气味;
(4)高温条件下,碳酸钙分解生成氧化钙和二氧化碳,高于反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:(1)①上述过程中,氯化镁和氢氧化钙反应生成氢氧化镁沉淀和氯化钙,属于复分解反应,氢氧化镁和稀盐酸反应生成氯化镁和水,属于复分解反应,电解氯化镁生成镁和氯气,属于分解反应,涉及反应的基本类型不包括化合反应和置换反应.
故填:ac.
②加入石灰乳时,氯化镁和氢氧化钙反应生成氢氧化镁沉淀和氯化钙,发生反应的化学方程式为:MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2.
故填:MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2.
(2)①如果将Ⅰ和Ⅱ的顺序颠倒,则所制得的精盐水中的溶质有氯化钠、反应生成的氯化钙.
故填:氯化钠、氯化钙.
②操作a、b均用到玻璃棒,其在操作b中的作用是使液体均匀受热,防止液体飞溅.
故答案为:使液体均匀受热,防止液体飞溅.
③Ⅳ中盐酸的作用是除去过量的碳酸钠和反应生成的氢氧化钠.
故答案为:除去过量的碳酸钠和反应生成的氢氧化钠.
(3)①上述Ⅰ、Ⅱ两个步骤中,氯化钠、水、氨气、二氧化碳等物质反应生成碳酸氢钠和氯化铵,反应的化学方程式是:NaCl+H2O+CO2+NH3═NaHCO3↓+NH4Cl.
故填:NaCl+H2O+CO2+NH3═NaHCO3↓+NH4Cl.
②鉴别铵态氮肥和尿素两种化肥的方法是:取样品适量分别与研钵中,加入氢氧化钙后研磨,产生刺激性气味的是铵态氮肥,无明显现象的是尿素.
故填:取样品适量分别与研钵中,加入氢氧化钙后研磨,产生刺激性气味的是铵态氮肥,无明显现象的是尿素.
(4)设反应生成氧化钙质量为x,
煅烧后质量减少了2.2t,说明反应生成了2.2t二氧化碳;
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,
56 44
x 2.2t
$\frac{56}{x}$=$\frac{44}{2.2t}$,
x=2.8t,
答:可制得氧化钙的质量是2.8t.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

实验一:重新取一洁净的试管和纯净的碳酸钠溶液,滴加酚酞试液,酚酞试液变红:用pH试纸测试,溶液的pH为11.
实验二:分别测试纯净碳酸钾、氯化钠、硫酸铜、硫酸钠、氯化铁、硝酸钾溶液的pH,实验结果纪录如下:
| 盐 | K2CO3 | NaCl | CuSO4 | Na2SO4 | FeCl3 | KNO3 |
| pH | 10 | 7 | 4 | 7 | 3 | 7 |
酸和碱都有强弱之分,盐酸、硫酸、硝酸是强酸,碳酸,醋酸等是弱酸.氢氧化钠、氢氧化钾是强碱,氢氧化铁、氢氧化铜是弱碱.
盐是酸碱中和的产物,强酸跟弱碱反应生成的盐叫强酸弱碱盐,强碱跟弱酸反应生成的盐叫强碱弱酸盐,强酸跟强碱反应生成的盐叫强酸强碱盐.
(1)小明由实验一得出的结论是碳酸钠溶液显碱性;实验二得出的结论是有些盐溶液呈中性;有些盐溶液呈碱性;有些盐溶液呈酸性.
(2)由实验二和查得的资料进行分析,你还能得出的结论是强酸弱碱盐呈酸性;强碱弱酸盐呈碱性;强酯强碱盐呈中性;酸碱指示剂只能检测出溶液的酸碱性;呈碱性的不一定是碱,呈酸性的不一定是酸.
| A. | 盐酸:制药 | B. | 氢氧化钠:改良土壤 | ||
| C. | 食盐:制烧碱 | D. | 硫酸铵:作化肥 |
| A. | +$\frac{M•x•c%}{98w}$ | B. | +$\frac{M•x•c%}{49w}$ | C. | +$\frac{x•c%}{w}$ | D. | +$\frac{M•y}{w}$ |
| 稀硫酸用量 | 剩余固体质量 |
| 第一次加入10g | mg |
| 第二次加入10g | 2.0g |
| 第三次加入10g | 1.5g |
| 第四次加入10g | 1.0g |
| 第五次加入10g | 0.6g |
| 第六次加入10g | 0.6g |
(2)计算整个实验过程中总共生成氢气的质量是多少?
(3)计算所用稀硫酸中H2SO4的质量分数?
| 序号 | 物质(括号内为杂质) | 除杂试剂 | 分离方法 |
| A | 硫酸铜溶液(硫酸) | 氧化铜 | 过滤 |
| B | NaOH溶液[Ca(OH)2溶液] | 二氧化碳 | 过滤 |
| C | 二氧化碳(一氧化碳) | 氢氧化钠溶液 | 洗气 |
| D | 二氧化锰粉末(碳粉) | 水 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |