题目内容
17. 屠呦呦因发现青蒿素(C15H22O5)荣获诺贝尔奖.青蒿素组成元素在元素周期表中的信息如图所示.下列说法正确的是( )
屠呦呦因发现青蒿素(C15H22O5)荣获诺贝尔奖.青蒿素组成元素在元素周期表中的信息如图所示.下列说法正确的是( )| A. | 青蒿素属于有机高分子化合物 | |
| B. | 青蒿素由15个C、22个H和5个O原子构成 | |
| C. | 三种元素的本质区别是相对原子质量不同 | |
| D. | 青蒿素中氧元素的质量分数为28.37% |
分析 A.根据有机高分子化合物的概念来分析;
B.根据物质的结构来分析;
C.根据元素的概念来分析;
D.根据青蒿素中氧元素质量分数的计算方法来分析.
解答 解:A.青蒿素的相对分子质量为12×15+1×22+16×5=282,而有机高分子化合物的相对分子质量大到几万甚至几十万,故错误;
B.青蒿素是由青蒿素分子构成的而不是由原子直接构成的,故错误;
C.元素的本质区别是核电荷数或质子数不同,故错误;
D.青蒿素中氧元素的质量分数为$\frac{16×5}{282}×100%$≈28.37%,故正确.
故选D.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
20.小明在做铁与硫酸溶液反应的实验时,发现生成的气体有刺激性气味,于是进行了探究.
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】(1)2Fe+6H2SO4(浓)$\frac{\underline{\;加热\;}}{\;}$Fe2(SO4)3+3SO2↑+6H2O
(2)SO2可使品红溶液的红色褪去
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫.
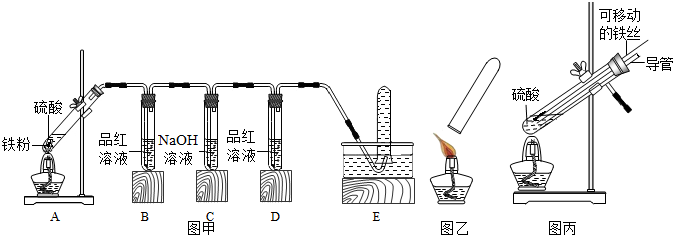
【实验探究】小明用图甲所示装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验.
请帮助小明完成下表:
【实验结论】铁与不同浓度的硫酸反应,生成的气体产物可能不同,当硫酸溶液浓度达到足够大时,生成的气体产物中有二氧化硫.
【交流反思】(1)写出实验三中铁与硫酸溶液反应的化学方程式Fe+H2SO4═FeSO4+H2↑.
(2)实验一中C装置的作用是吸收二氧化硫.
【拓展延伸】小明将A装置进行了如图丙所示的改进,试分析:增加的导管下端伸入液面以下的原因形成液封,防止生成的气体逸出;该导管所起的作用是平衡试管内外的压强,防止停止加热时液体倒吸入试管.

【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】(1)2Fe+6H2SO4(浓)$\frac{\underline{\;加热\;}}{\;}$Fe2(SO4)3+3SO2↑+6H2O
(2)SO2可使品红溶液的红色褪去
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫.
【实验探究】小明用图甲所示装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验.
请帮助小明完成下表:
| 实验现象 | |||||
| 硫酸溶液浓度 | B中品红溶液 | D中品红溶液 | 爆鸣实验 | A中生成气体成分 | |
| 实验一 | 98% | 褪色 | 不褪色 | 无爆鸣声 | 只有SO2 |
| 实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | 有SO2和H2 |
| 实验三 | 25% | 不褪色 | 不褪色 | 有爆鸣声 | 只有H2 |
【交流反思】(1)写出实验三中铁与硫酸溶液反应的化学方程式Fe+H2SO4═FeSO4+H2↑.
(2)实验一中C装置的作用是吸收二氧化硫.
【拓展延伸】小明将A装置进行了如图丙所示的改进,试分析:增加的导管下端伸入液面以下的原因形成液封,防止生成的气体逸出;该导管所起的作用是平衡试管内外的压强,防止停止加热时液体倒吸入试管.
8.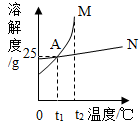 如图是M、N两种固体物质(不含结晶水)的溶解度曲线,下列说法错误的是( )
如图是M、N两种固体物质(不含结晶水)的溶解度曲线,下列说法错误的是( )
 如图是M、N两种固体物质(不含结晶水)的溶解度曲线,下列说法错误的是( )
如图是M、N两种固体物质(不含结晶水)的溶解度曲线,下列说法错误的是( )| A. | 图中A点表示M、N两种物质在tl℃时溶解度相等 | |
| B. | t2℃时,分别将M、N饱和溶液冷却到tl℃,所得溶液 的 溶质质量分数都为25% | |
| C. | M中含有少量N,通常采用冷却结晶的方法提纯M | |
| D. | t1℃时,M的溶液恒温蒸发10g水析出lg晶体,再恒温蒸发20g水将析出5g晶体 |
5.复方篙甲醚(C16H26O5)是一种治疗疟疾的有效药品.下列说法正确的是( )
| A. | 复方篙甲醚属于氧化物 | |
| B. | 复方篙甲醚由47个原子构成 | |
| C. | 复方篙甲醚的相对分子质量为298g | |
| D. | 复方篙甲醚中各原子的个数比是16:26:5 |
12.下列实验设计正确的是( )
| A. | 用托盘天平称取10.12g蔗糖 | B. | 用加热来降低水的硬度 | ||
| C. | 用pH试纸测定溶液pH值为5.6 | D. | 用碱石灰干燥二氧化碳 |
2.在我们的日常生活中涉及到许多变化.下列变化中不包含化学变化的是( )
| A. | 用石灰浆涂抹墙壁后,表面有水珠生成 | |
| B. | 在口中咀嚼米饭或馒头时感到有甜味 | |
| C. | 冰块制成冰雕 | |
| D. | 绿色植物的光合作用 |
9.家庭生活中处处有物质的变化,以下属于物理变化的是( )
| A. | 鲜牛奶变质 | B. | 酵母粉发酵 | C. | 洁厕精除垢 | D. | 钢丝球刷碗 |
6.在高温下,铁与水蒸气能发生反应生成一种常见铁的氧化物和一种气体.某化学学习小组的同学对此反应很感兴趣,在小组集体协作下设计了如图所示实验,以探究铁粉与水蒸气反应后的产物,也邀请你一起来完成下列探究:
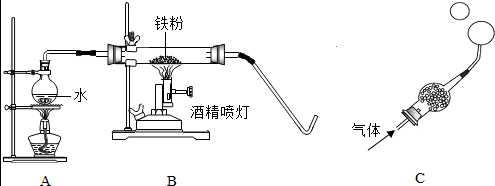
(1)A装置的作用是:提供水蒸气.
(2)探究生成的气体是什么?
【猜想与假设】猜想一:生成的气体可能是氢气;猜想二:生成的气体可能是氧气.
【实验探究】将生成的气体通入C装置.球形管里装有碱石灰干燥剂.导管口蘸些肥皂水(或洗涤剂溶液),控制气体流速,吹出肥皂泡.当肥皂泡吹到一定大时,轻轻摆动导管,肥皂泡脱离管口后,气泡上升.用燃着的木条靠近肥皂泡,有爆鸣声.
【推断】生成的气体是氢气.
(3)探究试管中剩余固体成分是什么?
【查阅资料】
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引.
【猜想与假设】猜想一:剩余固体是Fe和Fe3O4; 猜想二:剩余固体是:Fe3O4.
【实验探究】
【实验结论】铁与水蒸气反应的化学方程式为:3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.
【反思与交流】该黑色固体不可能是FeO、Fe2O3,理由是FeO不能被磁铁吸引,Fe2O3红棕色粉末且不能被磁铁吸引.

(1)A装置的作用是:提供水蒸气.
(2)探究生成的气体是什么?
【猜想与假设】猜想一:生成的气体可能是氢气;猜想二:生成的气体可能是氧气.
【实验探究】将生成的气体通入C装置.球形管里装有碱石灰干燥剂.导管口蘸些肥皂水(或洗涤剂溶液),控制气体流速,吹出肥皂泡.当肥皂泡吹到一定大时,轻轻摆动导管,肥皂泡脱离管口后,气泡上升.用燃着的木条靠近肥皂泡,有爆鸣声.
【推断】生成的气体是氢气.
(3)探究试管中剩余固体成分是什么?
【查阅资料】
| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
| 能否与盐酸反应 | 能 | 能 | 能 |
【猜想与假设】猜想一:剩余固体是Fe和Fe3O4; 猜想二:剩余固体是:Fe3O4.
【实验探究】
| 实验操作 | 实验现象及结论 |
取少量黑色固体于试管中,加入足量的稀盐酸 | 若固体全部溶解,没有气泡冒出,则猜想二正确;若固体全部溶解,有气泡冒出,则猜想一正确. |
【反思与交流】该黑色固体不可能是FeO、Fe2O3,理由是FeO不能被磁铁吸引,Fe2O3红棕色粉末且不能被磁铁吸引.