题目内容
19.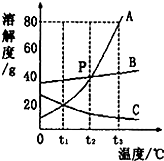 如图是 A、B、C三种物质的溶解度曲线,回答下列问题:
如图是 A、B、C三种物质的溶解度曲线,回答下列问题:(1)A物质在t3℃时溶解度为80g.
(2)P点表示t2℃时AB的溶解度相同.
(3)t2℃时,三种物质溶解度由大到小的顺序是A=B>C.
(4)如果A物质中混有少量B物质,可采取降温结晶(或冷却热饱和溶液)的方法得到较纯的A物质.
(5)除上述描述外,通过此曲线图你还能得到的信息是A的溶解度随温度升高而增大,且变化较大(合理均可).
分析 (1)据溶解度曲线可知某温度下物质的溶解度;
(2)溶解度曲线的交点表示该温度下两物质的溶解度相等;
(3)据溶解度曲线可比较同一温度下不同物质的溶解度大小;
(4)据物质的溶解度曲线可知物质的溶解度受温度影响情况,进而分析提纯物质的方法;
(5)据溶解度曲线可知物质的溶解度受温度影响情况等.
解答 解:(1)据图可以知道,A物质在t3℃时溶解度为80g;
(2)P点表示在t2℃时A和B的溶解度相等;
(3)t2℃时,三种物质溶解度由大到小的顺序是:A=B>C;
(4)A的溶解度随温度升高变化明显,B的溶解度受温度影响不大,所以若A物质中混有少量B物质,可用降温结晶或冷却热饱和溶液的方法提纯A;
(5)由溶解度曲线还可知:A的溶解度随温度升高而增大,B的溶解度受温度影响较小,C的溶解度随温度的升高而减少;
故答案为:(1)80g;
(2)t2℃时A和B的溶解度相等;
(3)A=B>C;
(4)降温结晶(或冷却热饱和溶液);
(5)A的溶解度随温度升高而增大,且变化较大(合理均可).
点评 本题考查了溶解度曲线的意义及其应用,完成此题,可以依据已有的知识进行,能较好考查学生分析、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.常温下,某气体难溶于水,密度比空气大,收集该气体可采用的方法是( )
| A. | 向上排空气法 | B. | 排水集气法 | ||
| C. | 排水集气法或向下排空气法 | D. | 排水集气法或向上排空气法 |
10. 等质量的M、N两种金属片,分别与相同浓度的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气的质量和反应时间的关系如图所示,下列叙述正确的是( )
等质量的M、N两种金属片,分别与相同浓度的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气的质量和反应时间的关系如图所示,下列叙述正确的是( )
 等质量的M、N两种金属片,分别与相同浓度的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气的质量和反应时间的关系如图所示,下列叙述正确的是( )
等质量的M、N两种金属片,分别与相同浓度的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气的质量和反应时间的关系如图所示,下列叙述正确的是( )| A. | 生成H2 的质量M<N | B. | N消耗的稀盐酸比M消耗的多 | ||
| C. | 相对原子质量较大的是N | D. | 产生H2 的快慢程度N>M |
14.铝在氧气中燃烧生成三氧化二铝,则参加反应的铝、氧气,生成的三氧化二铝的质量比是( )
| A. | 27:32:102 | B. | 54:32:102 | C. | 54:24:102 | D. | 108:96:204 |
4.材料与人类生活密切相关,下列物品的主要成分是由有机合成材料制成的是( )
| A. | 全毛羊毛衫 | B. | 塑料脸盆 | C. | 铝合金门窗 | D. | 玻璃杯 |
11.小方同学在迎中考体育锻练过程中,使用的下列物品中不含有机合成材料的是( )
| A. | 李宁橡胶底运动鞋 | B. | 纯棉T恤 | ||
| C. | 塑料水瓶 | D. | 腈纶背包 |
8.下列图象与对应描述相符的是( )
| A. | 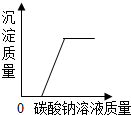 向氢氧化钙溶液中加入碳酸钠溶液 | |
| B. | 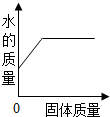 一定质量的稀硫酸中不断加入氧化铜固体 | |
| C. |  两份等质量的相同质量分数的稀硫酸中不断加入锌和铁 | |
| D. | 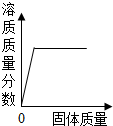 向一定温度下接近饱和的硝酸钠溶液中加入硝酸钠固体 |
9.硫酸铜是一种应用极其广泛的化工原料,易溶于水而不易溶于酒精;以下是某工厂用含铁废铜为原料生产胆矾(CuSO4•5H2O)和副产物石膏(CaSO4•2H2O)的生产流程示意图:
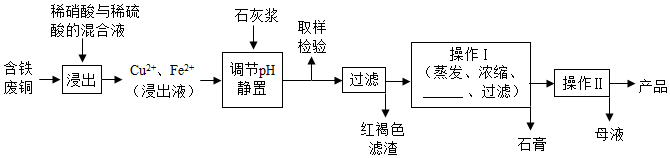
胆矾和石膏在不同温度下的溶解度(g/100g水)如表.
请回答下列问题:
(1)红褐色滤渣的主要成分是Fe(OH)3;
(2)含铁的废铜和稀硫酸反应的化学方程式Fe+H2SO4=FeSO4+H2↑;
(3)操作I最后温度应该控制在100℃左右;
(4)从溶液中分离出硫酸铜晶体的操作Ⅱ应为蒸发浓缩、冷却结晶、过滤、洗涤、干燥;晶体用无水乙醇作洗涤液而不用蒸馏水的原因是减少因晶体溶解造成的损失.

胆矾和石膏在不同温度下的溶解度(g/100g水)如表.
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
(1)红褐色滤渣的主要成分是Fe(OH)3;
(2)含铁的废铜和稀硫酸反应的化学方程式Fe+H2SO4=FeSO4+H2↑;
(3)操作I最后温度应该控制在100℃左右;
(4)从溶液中分离出硫酸铜晶体的操作Ⅱ应为蒸发浓缩、冷却结晶、过滤、洗涤、干燥;晶体用无水乙醇作洗涤液而不用蒸馏水的原因是减少因晶体溶解造成的损失.