题目内容
6.根据下列提供的试剂,判断不能发生反应的一组是( )| A. | Na2SO4溶液和Ba(NO3)2溶液 | B. | AgNO3溶液和金属铜 | ||
| C. | NaOH溶液和CuSO4溶液 | D. | Na2CO3溶液和Fe2O3 |
分析 根据复分解反应的发生条件,两物质交换成分生成物中必须有沉淀、气体或水,反应才能进行,据此进行分析判断即可.
解答 解:A、Na2SO4溶液和Ba(NO3)2溶液反应生成硫酸钡沉淀和硝酸钠,有沉淀生成,能发生复分解反应.
B、AgNO3溶液和金属铜,在金属活动性顺序中,铜排在银的前面故金属铜能AgNO3溶液反应置换出银;
C、NaOH溶液和CuSO4溶液反应生成硫酸钠和氢氧化铜沉淀,能发生复分解反应.
D、Na2CO3溶液和Fe2O3氧化铁不溶于水,不能交换成分,不能发生复分解反应.
故选D.
点评 本题难度不大,考查复分解反应发生的条件,掌握复分解反应的条件(生成物中有沉淀、气体或水)是正确解答此类题的关键.

练习册系列答案
相关题目
6.下列物质中.氯元素的化合价为+5价的是( )
| A. | HCl | B. | Cl2 | C. | KClO3 | D. | Cl2O7 |
7.生活中一些物质的近似pH如下.有关说法不正确的是( )
| 物质 | 醋酸 | 橘子汁 | 草木灰水 | 炉具清洁剂 |
| pH | 2.5 | 3.4 | 11.1 | 12.4 |
| A. | 草木灰水显碱性 | B. | 胃酸过多的人少吃橘子 | ||
| C. | 上述物质酸性最强的是炉具清洁剂 | D. | 醋酸能使紫色石蕊试液变红 |
4.下列物质中属于氧化物的是( )
| A. | NaOH | B. | C6H12O6 | C. | Al2O3 | D. | H2SO4 |
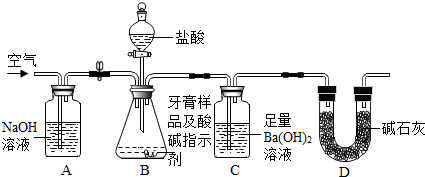
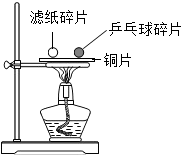 某化学学习小组利用如图设计方案来探究可燃物燃烧的条件.
某化学学习小组利用如图设计方案来探究可燃物燃烧的条件. 铜在工农业生产中应用广泛.请回答:
铜在工农业生产中应用广泛.请回答: