题目内容
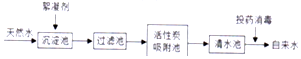
9.如图是某化工厂利用CaSO4制备(NH4)2SO4的工艺流程.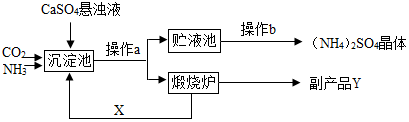
回答下列问题:
(1)向沉淀池中通气体时,通常先通入NH3后通CO2,目的是通入NH3后溶液显碱性,有利于吸收二氧化碳.
(2)沉淀池中主要反应:CO2+2NH3+CaSO4+H2O=(NH4)2SO4+M↓,则M为CaCO3.
(3)操作a、b中都用到的分离操作的名称是过滤.
(4)副产品Y在实验室中可用作干燥剂,可以干燥氢气等气体.
分析 (1)氨气能和水反应生成氨水,氨水显碱性;
(2)化学反应遵循质量守恒定律,即反应前后元素种类不变,原子种类、总个数和质量都不变;
(3)操作a、b中都用到的分离操作的名称是过滤,通过过滤能够把液体和固体分离;
(4)副产品Y是氧化钙,可以用作某些气体的干燥剂.
解答 解:(1)向沉淀池中通气体时,通常先通入NH3后通CO2,目的是通入NH3后溶液显碱性,有利于吸收二氧化碳.
故填:通入NH3后溶液显碱性,有利于吸收二氧化碳.
(2)由CO2+2NH3+CaSO4+H2O=(NH4)2SO4+M↓可知,反应前后氮原子都是2个,氢原子都是8个,硫原子都是1个,反应前碳原子是1个,反应后应该是1个,包含在M中,反应前氧原子是7个,反应后应该是7个,其中3个包含在M中,反应前钙原子是1个,反应后应该是1个,包含在M中,则M为CaCO3.
故填:CaCO3.
(3)操作a、b中都用到的分离操作的名称是过滤,通过过滤能够把液体和固体分离.
故填:过滤.
(4)副产品Y在实验室中可用作干燥剂,可以干燥氢气、氧气、甲烷等气体.
故填:氢气.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.草酸镍晶体(NiC2O4•2H2O)可用于制镍催化剂.某小组用废镍催化剂(成分为Fe2O3、Ni、Fe、SiO2等)制备草酸镍晶体的部分实验流程如图1:
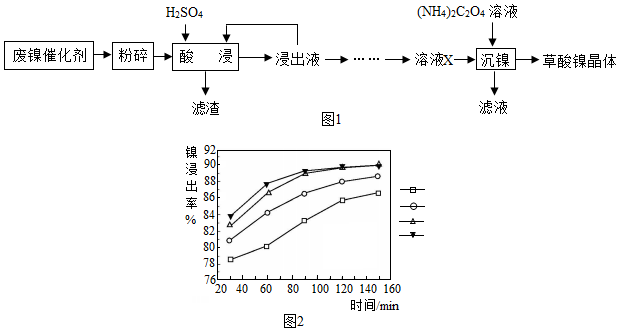
已知:①Ni能和稀H2SO4反应.
②相关金属离子生成氢氧化物沉淀的pH如表
③H2O2能将Fe2+氧化为Fe3+
(1)废镍催化剂“粉碎”的目的是增大与硫酸的接触面积,加快反应速率.
(2)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图2,“酸浸”的适宜温度与时间分别为C(填字母).
A.30℃、30min B.90℃、150min C.70℃、120min D.90℃、120min
(3)“酸浸”中发生的复分解反应方程式为Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
(4)“浸出液”得到“溶液x”过程中,加入试剂先后顺序是A(填字母)
A.先加H2O2溶液,再加NaOH溶液 B.先加NaOH溶液,再加H2O2溶液
加NaOH溶液调节pH3.2~6.7(填范围),充分反应后得到滤渣的操作是过滤,该操作中所用到的玻璃仪器有玻璃棒、烧杯和漏斗.
(5)将“沉镍”工序:①主要过程为:蒸发浓缩、降温结晶、过滤,所得固体用75%乙醇洗涤、110℃下烘干,得草酸镍晶体.
②用75%乙醇洗涤的目的是洗去杂质、减少草酸镍晶体的损失;
③烘干温度不超过110℃的原因是防止草酸镍失去结晶水.

已知:①Ni能和稀H2SO4反应.
②相关金属离子生成氢氧化物沉淀的pH如表
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Ni2+ | 6.7 | 9.5 |
(1)废镍催化剂“粉碎”的目的是增大与硫酸的接触面积,加快反应速率.
(2)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图2,“酸浸”的适宜温度与时间分别为C(填字母).
A.30℃、30min B.90℃、150min C.70℃、120min D.90℃、120min
(3)“酸浸”中发生的复分解反应方程式为Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
(4)“浸出液”得到“溶液x”过程中,加入试剂先后顺序是A(填字母)
A.先加H2O2溶液,再加NaOH溶液 B.先加NaOH溶液,再加H2O2溶液
加NaOH溶液调节pH3.2~6.7(填范围),充分反应后得到滤渣的操作是过滤,该操作中所用到的玻璃仪器有玻璃棒、烧杯和漏斗.
(5)将“沉镍”工序:①主要过程为:蒸发浓缩、降温结晶、过滤,所得固体用75%乙醇洗涤、110℃下烘干,得草酸镍晶体.
②用75%乙醇洗涤的目的是洗去杂质、减少草酸镍晶体的损失;
③烘干温度不超过110℃的原因是防止草酸镍失去结晶水.
4.下列成语或典故中,涉及化学变化的是( )
| A. | 滴水成冰 | B. | 大海捞针 | C. | 百炼成钢 | D. | 刻舟求剑 |
1.推理是化学学习的一种常用方法,下列推理说法正确的是( )
| A. | 中和反应生成了盐和水,生成盐和水的反应是中和反应 | |
| B. | 氧气能使带火星的木条复燃,不能使带火星的木条复燃的气体一定没有氧气 | |
| C. | 纯碱溶液显碱性,所以纯碱属于碱类物质 | |
| D. | 单质是只含一种元素的纯净物,只含有一种元素的纯净物是单质 |
18.归纳和推理是化学学习的一种重要思维方法,以下类推结果与实际相符合的是( )
| A. | 有机化合物都含有碳元素,含有碳元素的化合物不一定是有机物 | |
| B. | 碳酸盐能与盐酸反应产生气体,能与盐酸反应生成气体的物质一定是碳酸盐 | |
| C. | 铝与盐酸反应生成AlCl3和H2,则金属铁与盐酸反应生成FeCl3和H2 | |
| D. | 酸碱中和反应有水生成,有水生成的反应一定是中和反应 |
19. 如图是甲、乙、丙三种物质的溶解度曲线.下列有关说法正确的是( )
如图是甲、乙、丙三种物质的溶解度曲线.下列有关说法正确的是( )
 如图是甲、乙、丙三种物质的溶解度曲线.下列有关说法正确的是( )
如图是甲、乙、丙三种物质的溶解度曲线.下列有关说法正确的是( )| A. | 甲、乙、丙三种物质中甲的溶解度最大 | |
| B. | t2℃时,10g水中加10g 甲,充分搅拌可得20g甲溶液 | |
| C. | 其它条件不变,升高温度可使用甲的饱和溶液变成不饱和溶液 | |
| D. | t1℃时甲、乙、丙三者的溶液其溶质质量分数相等 |

 ”、“
”、“ ”、“
”、“ ”代表不同原子,产物D为次氯酸(HClO),有杀菌消毒作用.
”代表不同原子,产物D为次氯酸(HClO),有杀菌消毒作用.